“重医”大反转|重庆食药监局首度开腔:暂未发现违纪,举报人所留信息不实
在经历“疫苗事件”后,医药板块一夜之间便成了众多投资者口中的“雷区”,稍有消息,该板块顷刻“摇摇欲坠”。比如8月30日疯传的“重庆医药工业研究院制药公司严重违反药品管理法”事件,A、H两市的医药板块同时下挫1.55%,而因涉及公司属复星医药(02196)孙公司,复星医药的股价也遭遇拖累。
可“事实”真如业界所传“踩雷”么?还没来得及深入思考,8月31日早间,故事似乎便出现反转。智通财经APP翻阅重庆市食品药品监管局公开信箱时发现,该局更新了调查进展情况并公开回复举报人信息。

其称,“我局组织的主要由国家药品GMP检查员组成的调查组,正对举报的问题开展深入调查;驻局纪检监察组对举报反映的我局监管人员接受吃请、收受红包的情况进行了初步核实,暂未发现有违法违纪问题;积极主动与举报人进行联系,但发现其所留信息不是举报人真实信息,目前我们一直未能联系上实际举报人。”
简单理解,就是初步调查后,重庆医药工业研究院制药公司并没有违法违纪,且举报人留的信息不真实,根本没法联系到。说好的实名举报呢?
事实上,重庆市食品药品监管局作出回应的前一晚,复星医药高层也在第一时间针对信件里面的内容做严格自查核实与说明。

公告称,重庆医药工业研究院有限责任公司及其制药公司重庆医工院制药有限责任公司主要从事仿制药原料药和中间体的研发、生产和销售。2017年度,重庆医工院(合并口径)实现营业收入人民币7780万元,占复星医药集团2017年度营业收入的0.42%。
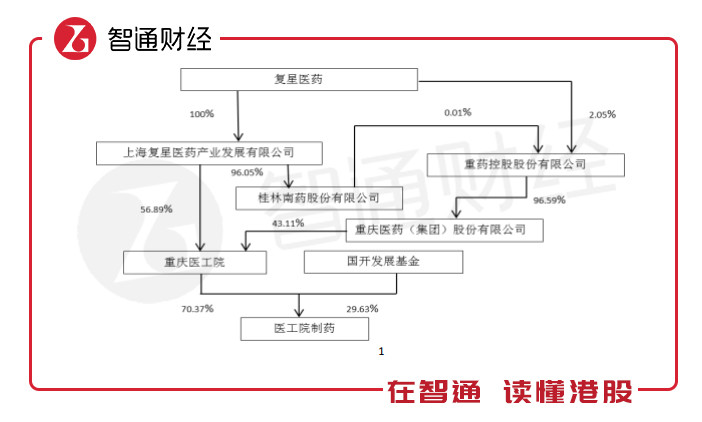
主要核实内容说明如下:
1、2016年5月美国食品药品监督管理局(以下简称“FDA”)对重庆医工院南岸区涂山路工厂进行检查,针对其QC实验室原料药检查中所发现的实验室数据规范性不足出具警告信、提出整改要求,详情请见本公司于 2017 年3月2日刊发的相关公告。根据上述整改要求,已对重庆医工院时任主要领导及相关责任人员进行了严肃处理调整,并在积极推进相关整改工作,力争尽快通过FDA现场检查。
2017年11月,FDA针对医工院制药(长寿区新场地)的质量体系进行批准前检查。检查后对于原料药阿立哌唑提出一条483缺陷,该缺陷主要针对阿立哌唑检测时所产生的无效OOS(偏差调查)不充分。目前,医工院制药已经在FDA的规范指引下展开整改。
2、此外,根据医工院制药自查,现有产品均根据已批准的工艺进行生产。在生产过程中,对于生产工艺的调整均经相关药监部门批准或备案。
3、根据经营的需要,重庆医工院于2016年向医工院制药转移了阿立哌唑、培美曲塞二钠产品批件,于2018年转移了蔗糖铁产品批件,并已通过药监部门的现场检查和批准。
4、医工院制药的原料药阿立哌唑目前在进行工艺变更的申报,2018年提供给上海中西三维药业有限公司的产品仅作为其制剂研究之用。
5、重庆食药监局已就该信件所反映的内容开展相关调查,并已于2018年8月23日对重庆医工院进行了飞行检查,飞行检查的结果尚待结论性意见。
针对“重医”事件与重庆的整体布局,智通财经APP也连线到了复星医药总裁兼CEO吴以芳。他表示,“一直以来,复星医药坚持规范管理和创新发展。公司将密切关注信件所涉事项的后续进展,并及时与相关方保持有效沟通;同时,将进一步要求下属企业强化自律管理。”




 扫码下载智通APP
扫码下载智通APP