港交所生物科技周来袭,11家生物医药公司排队IPO
本文来源微信公众号“医药观澜”。
近日,港交所发布了生物科技周预告。数据显示,截至今年4月底,9家生物科技公司发行新股,包括百济神州(06160)、信达生物(01801)、华领医药(02552)、歌礼制药(01672)等一批具有代表性的国内创新企业。其中没有营业收入的公司有7家。上市新政实施一年以来,香港已经成为全球第二大生物科技上市中心。
香港生物科技生态圈正在慢慢成形,这个市场也吸引了越来越多的行业内的专业投资者、分析师和顾问。当然,这个市场的主角也从未缺席。预告显示,截至4月30日,共有11家生物技术和医疗保健公司在港交所提交上市申请,其中9家公司位于中国。本文将盘点其中8家从事新药研发的创新药企,这些企业依次有复宏汉霖、盟科生物、迈博医药、亚盛医药、东曜药业、豪森药业、和黄中国医药、康蒂尼药业。
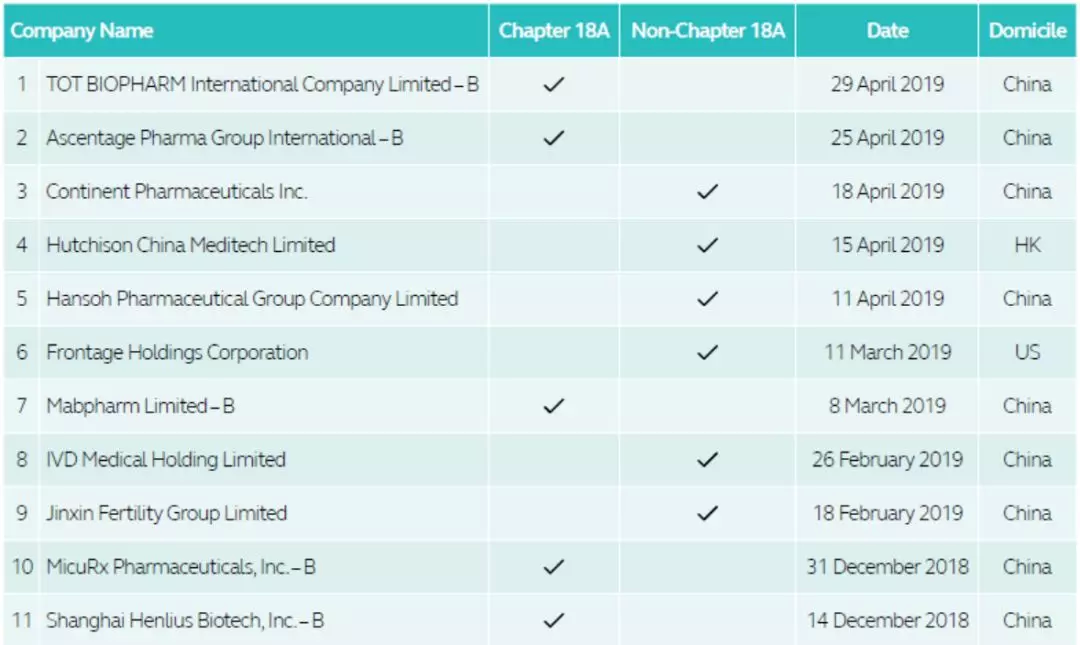
▲图片来源:HKEXnews website
复宏汉霖(Shanghai Henlius Biotech)
创建于2010年的复宏汉霖,主要致力于应用前沿技术进行生物类似药、生物改良药以及创新型单抗的研发及产业化。该公司在中国上海、台北和美国加州均设有研发中心,产品覆盖肿瘤、自身免疫性疾病等领域。
复宏汉霖刚刚递交IPO申请,拟于港交所主板上市
截至目前,复宏汉霖拥有丰富的在研产品管线,累计获得全球范围内29个临床试验许可。其中,中国大陆19个,中国台湾3个,美国3个,欧盟、澳大利亚、乌克兰和菲律宾各1个。复宏汉霖在中国还获得了两项单抗联合疗法的临床试验批准,分别是HLX10(PD-1单抗)联合HLX07(抗EGFR单抗),HLX10联合HLX04(抗VEGF单抗)。
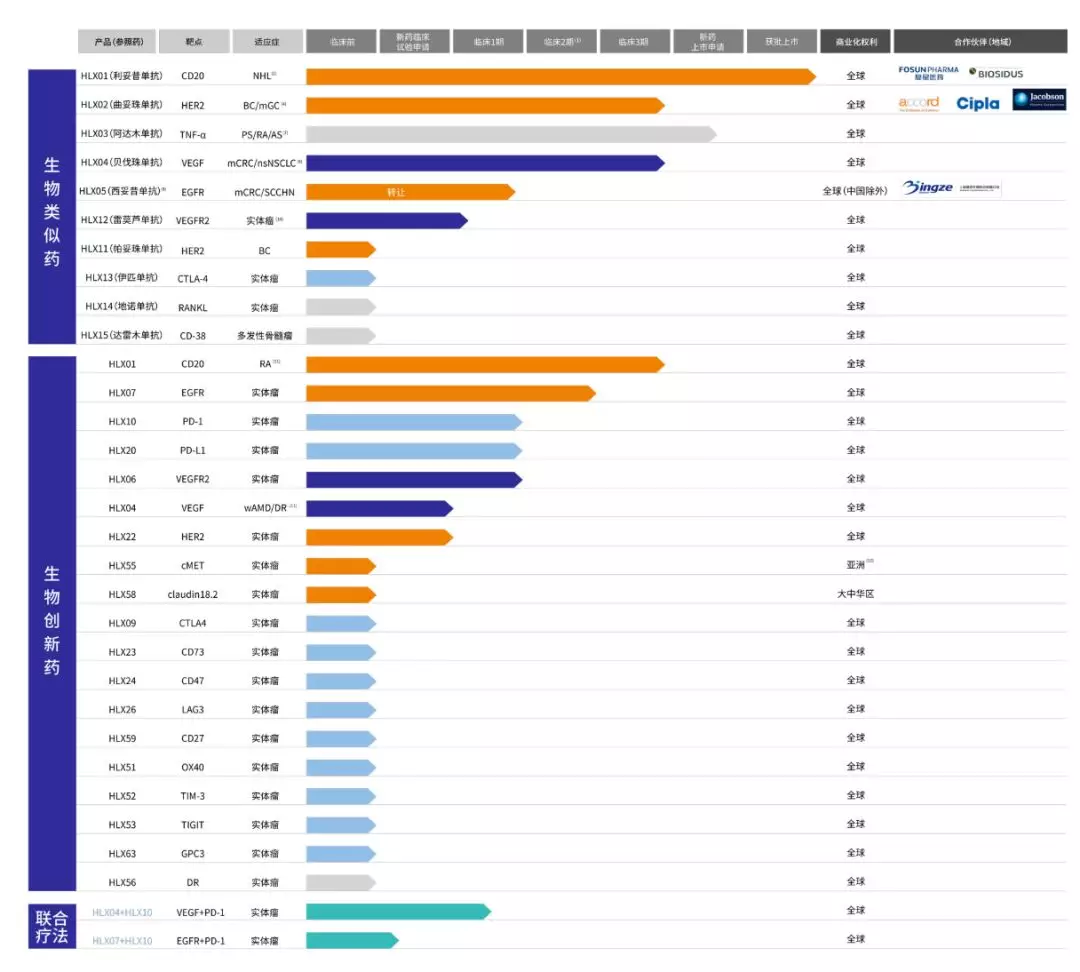
▲复宏汉霖在研产品(图片来源:复宏汉霖官网)
今年2月,复宏汉霖旗下首款产品——自主研发的首个单抗药物汉利康(利妥昔单抗注射液)获得国家药品监督管理局批准上市,用于治疗非霍奇金淋巴瘤。值得注意的是,作为国内首个以原研利妥昔单抗为参照药,按照生物类似药途径开发和申报生产的汉利康,获批了原研利妥昔单抗在中国的所有适应症。
不久后,复宏汉霖的HLX03(阿达木单抗注射液)和HLX02(曲妥珠单抗注射液)先后获得国家药品监督管理局新药上市申请受理。其中,阿达木单抗注射液还被药品审评中心纳入优先审评程序。
盟科生物(MicuRx Pharmaceuticals)
2007年成立的盟科生物,是一家处于临床阶段的生物医药公司,专注于发现、开发及商业化治疗多重耐药(MDR)“超级细菌”感染的新型抗生素,在美国加州旧金山市郊和中国上海设有研发实验室。
信达生物、盟科医药正式向港交所递交上市申请
盟科生物在中美两地科学家凭藉研发新型抗生素的丰富经验,构建了由四款抗菌新药组成的研发管线(contezolid(MRX-I)、contezolid acefosamil(MRX-4)、MRX-8及MRX-10),旨在治疗世界卫生组织“超级细菌”名单上所列的多个病原体。
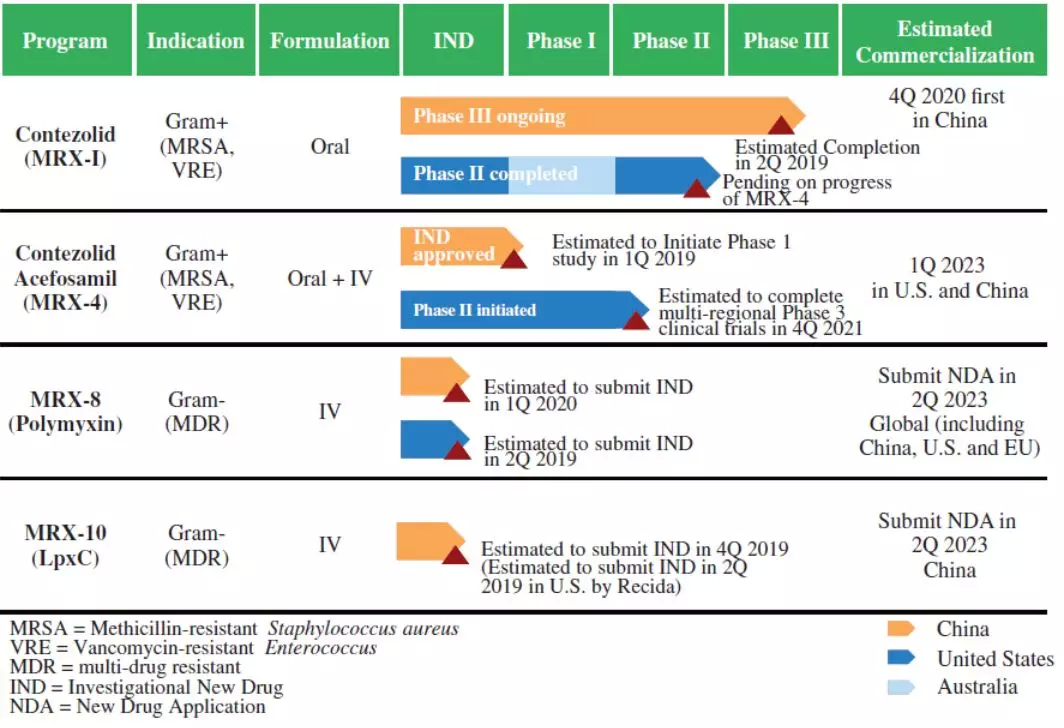
▲盟科生物在研产品(图片来源:盟科生物官网)
其中,contezolid(MRX-I)是由盟科生物自主研发的新型噁唑烷酮类抗生素,已获专利授权,并处于3期临床试验阶段。在中国、美国及澳洲进行的临床前及临床研究数据显示,contezolid具有治疗严重多重耐药革兰氏阳性细菌感染的潜力。
2018年,contezolid(MRX-I)和其前药contezolid acefosamil(MRX-4)获得美国FDA授予的快速通道资格和合格感染疾病产品(QIDP),用于治疗急性细菌皮肤和皮肤组织感染(ABBSSI)。
今年2月,盟科生物宣布其contezolid acefosamil在美国的2期临床顺利完成首例患者入组,这一新药将用于治疗由革兰氏阳性菌,包括甲氧西林金黄色葡萄球菌(MRSA)和耐万古霉素肠球菌(VRE)导致的急性皮肤和皮肤组织感染(ABSSSI)。
迈博医药(Mabpharm Limited)
成立于2015年的迈博药业,是一家中国生物医药公司,专注于治疗癌症和自身免疫性疾病的新药及生物类似药的研发和生产。该公司拥有多项核心技术专利,包括抗体工程及人源化技术、高表达载体构建技术、高效克隆筛选技术,以及专有研发动物模型。
近日,港交所最新消息,迈博药业已在5月20日正式开始招股。IPO招股价为每股1.5~1.95港元,集资总额上限为15.28亿港元,预计5月31日正式挂牌上市。
迈博药业正式登陆港交所,拟募资15亿港元
根据上市公告,迈博药业研发管线包括9种单克隆抗体药物,其中处于3期临床试验的核心产品有3个,分别是奥马珠单抗(CMAB007)、西妥昔单抗(CMAB009)和英夫利昔单抗(CMAB008)。另外2项已获批临床试验的候选药物分别是曲妥珠单抗(CMAB809)和纳武单抗(CMAB819)。

▲迈博药业在研产品(图片来源:迈博药业上市公告)
根据上市公告,该公司计划分别在2020年第一季度、2019年第四季度及2021年第四季度完成提交CMAB007、CMAB008及CMAB009的新药上市申请。
亚盛医药(Ascentage Pharma Group International)
成立于2009年的亚盛医药,是一家全球领先的处于临床阶段的新药研发企业,总部位于苏州。该公司致力于在肿瘤、乙肝及与衰老相关的疾病等治疗领域开发创新药物,包括难以靶标的蛋白-蛋白相互作用抑制剂(PPIs)和下一代酪氨酸激酶抑制剂(TKIs)。
亚盛医药递交港股上市申请,3大抗癌药有望获资本助力
亚盛医药已构建丰富的产品布局,到目前为止,8个产品正处于临床开发阶段,20个正进行的临床试验和18个在全球范围内提交的INDs。其中,APG-1252、APG-2575、以及HQP1351是亚盛医药研发管线中的核心产品。
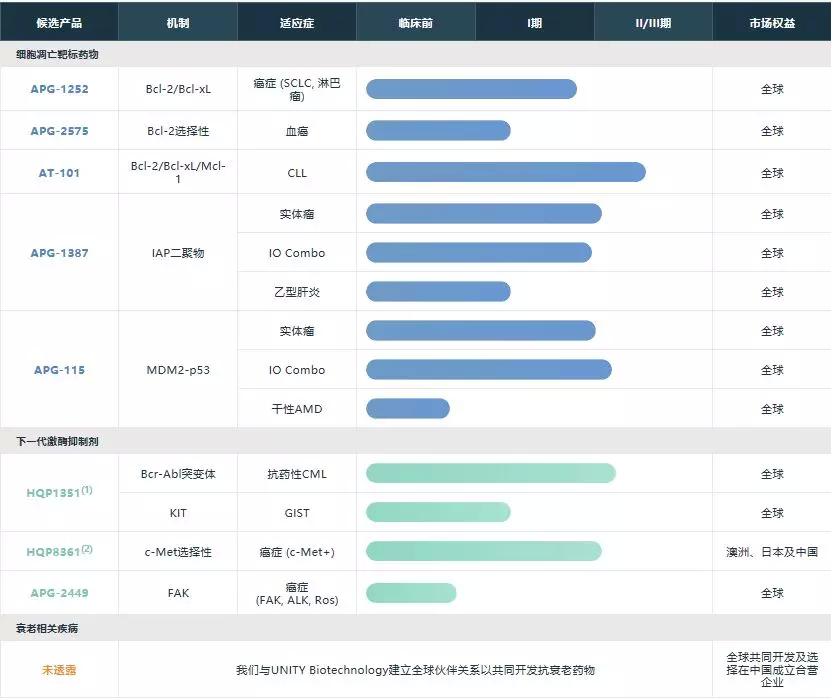
▲亚盛医药在研产品(图片来源:亚盛医药官网)
今年4月,亚盛医药宣布与君实生物达成临床合作,双方将针对亚盛医药特有的细胞凋亡抑制蛋白(IAP蛋白)抑制剂APG-1387与君实生物的抗PD-1单抗特瑞普利单抗的联合用药在中国大陆进行临床探索,治疗包括肿瘤(实体瘤与血液瘤),特别是难治性肿瘤、药物耐受性肿瘤等和其他双方另行确定的适应症。
APG-1387为新一代凋亡蛋白抑制因子(IAP)高效特异性抑制剂,主要通过模拟内源性Smac分子降解IAPs来诱导和加速细胞凋亡的进程,用于治疗晚期实体瘤及慢性HBV感染。目前,APG-1387作为单一药物已在中国和澳大利亚完成针对实体瘤的临床1期剂量爬坡试验,并正在美国开展与PD-1抗体联合治疗晚期实体瘤的1b试验。
此前,亚盛医药还与UNITY Biotechnology、嘉和生物、MD Anderson癌症中心等多家机构达成战略合作。
东曜药业(TOT BIOPHARM International Company Limited)
东曜药业为台湾东洋药品于2010年在苏州园区投资设立的全资子公司,是一家专业从事抗肿瘤新药研发、生产和市场营销的高新技术企业,核心药物包括特殊剂型药物、生物药、创新生技药物三大类抗癌症基因治疗药物。
东曜药业递交港交所上市申请,开发抗癌基因治疗新药
根据东曜药业招股书,该公司共有7个在研生物药和5个在研化学药。其中4款生物药目前处于临床阶段,包括处于3期临床的TAB008,以及处于1期临床的TAD011、TAB014和TAA013。另外3款生物药正在进行CMC或BE研究。据悉,该公司计划在2020年下半年启动3款小分子药物的商业化。
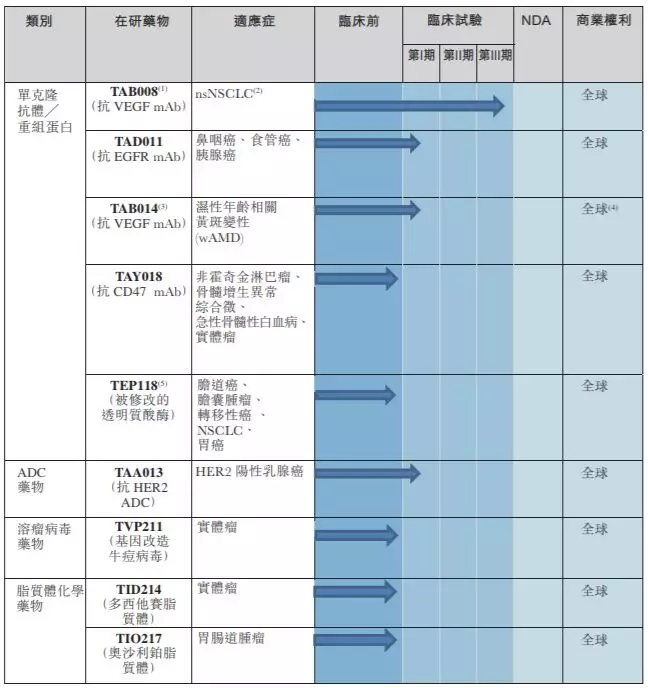
▲东曜药业研发管线1(图片来源:东曜药业招股书)
其中,TAB008是东曜药业的核心产品,也是该公司在研产品线中进展最快的一个。这是一种抗VEGF mAb药物和贝伐珠单抗生物类似药,预计将在今年完成3期试验,在2020年底至2021年推出。

▲东曜药业研发管线2(图片来源:东曜药业招股书)
2018年8月,东曜药业宣布完成1.02亿美元B轮融资。同年11月,东曜药业苏州工厂隆重开业。目前,其拥有一个近1000平方米的符合GMP要求的生物药中试厂房,包括了抗体生产区域、病毒生产区域和制剂分装区域等三个功能区域。
豪森药业(Hansoh Pharmaceutical Group Company Limited)
豪森药业(瀚森制药)成立于1995年,致力于中枢神经系统、抗肿瘤、抗感染、糖尿病、消化道和心血管六大领域。该公司在江苏连云港、上海张江分别建有研发中心,并形成包括药学研究、临床前研究、临床研究和注册申报的完整研发体系。
豪森药业再次递交IPO申请;康立明生物完成3亿元B轮融资
豪森药业主要布局于治疗发病率高的实体瘤以及治疗方案相对有限的血液肿瘤,包括核心产品普来乐、泽菲、昕维、昕美,以及具有强大增长潜力的主要产品昕泰。其在国内多重耐药性革兰氏阳性细菌抗生素市场中也排名靠前,包括四种主要产品,核心产品泽坦、以及具有强大增长潜力的主要产品迈灵达、恒捷、恒森。

▲豪森药业研发管线2(图片来源:豪森药业招股书)
目前,豪森药业在研1.1类新药包括:2型糖尿病新药(聚乙二醇洛塞那肽),甲磺酸氟马替尼,乙肝新药HS-10234和非小细胞肺癌(NSCLC)第三代分子靶向药物HS-10296。根据豪森药业的规划,其将在2019年至2020年推出近30种在研药物,其中包括15种具有高增长潜力的重点在研药物。
和黄中国医药(Hutchison China Meditech Limited)
和记黄埔中国医药科技有限公司(Chi-Med,下称和黄中国医药)是一家创新的生物制药公司,主要开发靶向疗法和免疫疗法的癌症药物。4月15日,和黄中国医药在香港交易所递交招股书。此前,该公司已经在英国AIM证券交易所和美国纳斯达克上市。
今日,和黄中国医药递交港交所上市申请!
值得注意的是,和黄中国医药旗下治疗转移性结直肠癌的靶向药,同时也是我国第一个国产抗肿瘤新药——呋喹替尼,已于2018年11月获批上市。根据招股书,除了呋喹替尼,该公司的沃利替尼和索凡替尼也有希望在未来两年内获批上市。
其中,沃利替尼是针对全球肺癌、肾癌、胃癌及前列腺癌药物开发领域或市场潜在同类首创的选择性MET抑制剂。索凡替尼是一种口服小分子抑制剂,靶点为VEGFR1、2及3、成纤维细胞生长因子受体1(或FGFR1)及集落刺激因子-1受体(CSF-1R),可同时阻断肿瘤血管生成和免疫逃逸。
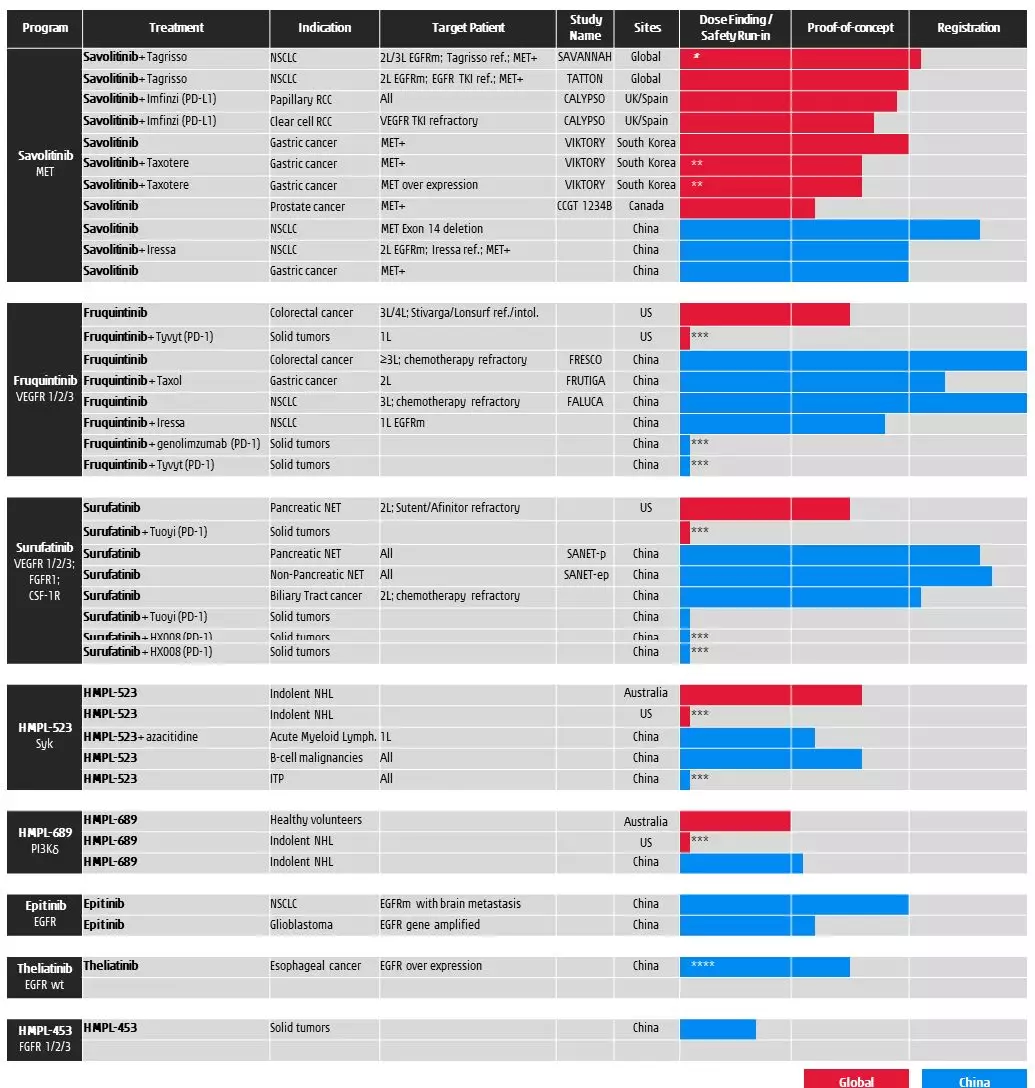
▲和黄中国医药在研产品(图片来源:和黄中国医药官网)
目前,和黄中国医药共有8个抗癌类候选药物进入临床阶段,其中5种已经或将要开始全球临床开发,正在中国及全球进行30多项临床试验。
招股书显示,和黄中国医药拟将此次上市募集资金用于推进公司药物沃利替尼、呋喹替尼以及索凡替尼的最后阶段临床项目注册实验及可能提交新药申请,推进该公司临床项目进入全球及中国的注册研究等。
研发创新药业务之外,和黄中国医药还经营处方药和消费保健品的销售业务。
康蒂尼药业(Continent Pharmaceuticals)
成立于2002年的康蒂尼药业,是一家专业开发孤儿药(针对治疗罕见病而开发的药剂)的公司,其在中国孤儿药市场中特发性肺纤维化(IPF)药物治疗领域具有一定领先优势。该公司的研发团队位于北京及上海,分为三个团队,分别专注于临床前研究(细胞研究及动物研究)、发展研究(化学、生产和控制)及临床发展。
新股速递丨康蒂尼药业,专注孤儿药的佼佼者
2018年,中国将IPF列入第一批《罕见病目录》中。康蒂尼药业的目标是利用其在中国IPF治疗药物市场现有的主导地位,以进一步开发、制造及分销用于治疗器官纤维化及其他罕见病的药品。
目前,康蒂尼药业的在研产品包括4款。其中,肝纤维化产品F351的2期临床试验预计将在今年完成,在美国被定义为罕见病的肝功能衰竭治疗产品F573正在准备启动1期临床试验。另外,该公司还获得了针对罕见病APL的他米巴维汀在中国的独家销售许可,预计将在今年获得国家药监局的进口药品许可。
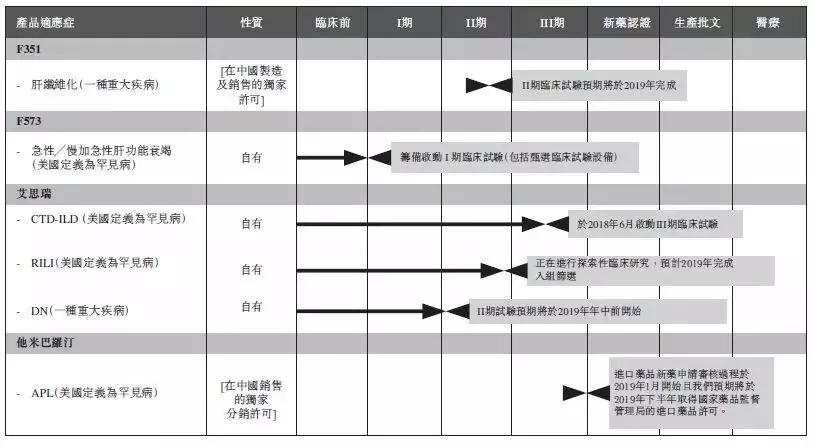
▲康蒂尼药业在研产品(图片来源:康蒂尼药业招股书)
康蒂尼药业主要产品艾思瑞(吡非尼酮胶囊),在2011年9月获得国家食品药品监督管理局颁发的1.1类新药证书,并于2014年上市销售,这是我国第一个治疗肺纤维化的药物。
此外,康蒂尼药业还开发并生产的产品有前列舒丸、复方川芎酊、罗红霉素片、阿昔洛韦片、奥美拉唑钠肠溶片、盐酸西替利嗪胶囊、氨酚伪麻那敏咀嚼片、吲达帕胺片等多个药品。(编辑:刘瑞)



 扫码下载智通APP
扫码下载智通APP