回望2019 :你不可错过的10大生物制药行业新闻
本文来自微信公众号“医药魔方”。原文标题《回望2019 :你不可错过的10大生物制药行业新闻》。
近日,BioSpace回顾了2019年10大新闻事件,本文对此进行编译,以飨读者。
Biogen的阿尔兹海默症新药
在过去的几年里,随着多家公司接连宣告阿尔兹海默症药物的研发失败,Biogen(BIIB.US)的aducanumab成为了最后的希望。
然而,2019年3月,Biogen及其合作伙伴日本生物制药公司Eisai(卫材)宣布:将停止针对aducanumab治疗阿尔茨海默氏症轻度认知障碍患者的两项全球III期临床试验ENGAGE和EMERGE,以及EVOLVEII期试验和PRIME Ib期长期试验。其原因在于独立数据监测委员在对这些试验进行无效性分析(futility analysis)后表示,很难达到其主要终点。 10月22日,这两家公司却再次宣布,EMERGE III期试验中aducanumab高剂量组达到其主要终点,且高剂量组部分患者在接受药物治疗后,在包括记忆力、方向感和语言等在内的认知和功能指标上有了明显改善,并在生活活动方面也表现明显益处。该公司在与美国FDA进行进一步地讨论后表示,计划将在2020年初提交生物制品许可上市申请,并将继续与包括欧洲和日本在内的国际市场监管机构进行协商。 12月5日,Biogen公司在美国圣地亚哥举行的第12届阿尔兹海默症临床试验(CTAD)会议上,公开了aducanumab试验的全部数据。学界和投资界并没有被这一消息冲昏头脑,大多数人仍保持审慎态度。他们认为尽管出现了一些让人令人激动的积极数据,但两项试验中仍存在令人担忧的安全信号和混合结果,可能影响FDA是否批准其上市申请。 aducanumab为治疗阿尔兹海默症提供了新的希望,但这一新药的“过山车式经历”仍在继续……
Keytruda成为肿瘤治疗的基石
今年6月,默沙东(MRK.US)首席商务官Frank Clyburn在5年来首个投资者日会议上表示,在不久的未来,Keytruda(帕博利珠单抗)将成为一种基础性的癌症治疗方法。“目前我们的临床试验涉及到了25种不同类型的癌症……而Keytruda正在改变当今患者的治疗方式。”尽管彼时许多分析师对该公司过度依赖该产品而感到担忧,但随着Keytruda适应症的不断获批,Clyburn的这些预言被证明不是为了哄抬股价而夸下的海口。
有分析家认为,Keytruda即将取代Humira(2023年失去美国市场专利保护)在2025年之后成为世界上销量最大的药物。并且,Keytruda 自2014年以来已经获得了20多项适应症批准,随着2020年的到来,Keytruda也可能会获得更多的批准,有望在未来获得更多收入。 Keytruda在中美两国的适应症获批情况
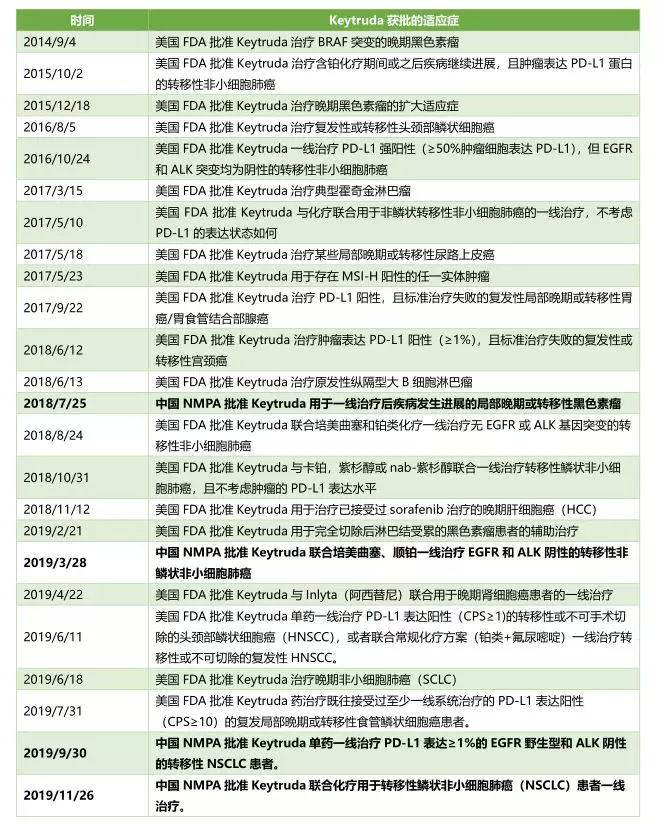
(注:不完全统计)
大型并购年
并购是日新月异的生物技术行业不变的主题。2019年,随着一些并购案的发生,行业格局也发生了几次大规模的变化。
2019年交易并购TOP10
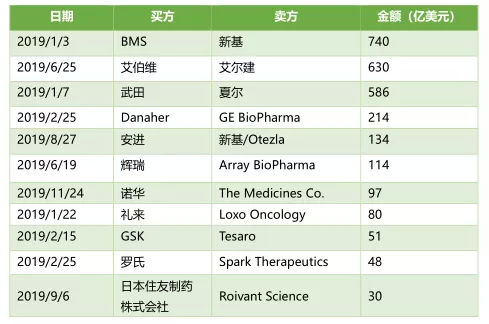
首先不得不提及的是,1月,BMS宣布将以740亿美元收购Celgene。这两家制药巨头的“强强联手”创造了肿瘤学、血液学、免疫学和心血管疾病领域的巨擘。自合并以来,BMS先后获批了一些药物上市,其中包括由Celgene开发,已被FDA批准用于治疗患有β地中海贫血症的成年患者的Reblozyl(luspatercept-AAMT)。 6月,AbbVie宣布斥资630亿美元收购肉毒杆菌生产商艾尔建(Allergan)。达成最终交易协议时,艾伯维方面表示,艾尔建现有管线和产品的增加将立即为公司的产品布局带来更大的效益规模,以减少目前对重磅药物Humira的过度依赖。自合并后,该公司将在免疫学、血液肿瘤学、医学美学、神经科学、妇女健康、眼睛护理和病毒学方面拥有一些产品的特许经营权。 尽管以上两个事件是2019年最大手笔的并购案,但还有一些并购案,也在影响着整个生物技术领域的风云变化。例如:Mylan与辉瑞(PFE.US)普强(Upjohn)的合并。这一新公司将通过整合原两家公司高度互补的业务,进一步拓展市场。全新的产品管线中将出现许多知名品牌,如预计Epi-Pen,Viagra,Lipitor,Celebrex等,预计将在2020年收入达到200亿美元。
一项30亿美元的交易
2019年1月, BMS豪掷740亿美元收购Celgene成为本年度最大手笔的交易。9月,日本住友制药株式会社(Sumitomo Dainippon Pharma)与Roivant Science公司所达成的一项高达30亿美元的交易也颇受圈内人的关注。
日本住友制药以30亿美元的预付款买下Roivant Sciences公司旗下5家“Vant系”子公司,同时,住友制药还将获得Roivant公司10% 的股份,以及收购另外6家企业的选择权。
根据交易细节披露,日本住友制药将新建一家公司,将已收购的Myovant Sciences (女性健康和前列腺癌)、Urovant Sciences (泌尿系统疾病)、Enzyvant Therapeutics (儿童罕见疾病)、Altavant Sciences (呼吸系统罕见疾病) ,以及Spirovant Sciences(囊性纤维化的基因疗法)这5家公司纳入到统一管理中。同时,这家新公司将由前基因泰克高管、Roivant的执行主席Myrtle Potter暂为管理运营。
此外,除了30亿美元的预付款,日本住友制药还将需要为Myovant Sciences公司提供3.5亿的贷款,用于治疗子宫肌瘤临床III候选药物relugolix的后续研究及上市申请;以及为Urovant Sciences公司提供2亿美元的贷款,用于膀胱过度活动症药物vibegron的后续开发。
未来,如果日本住友制药行使继续收购其他6家公司的选择权,还有望在2020年到2022年间获得超过25种在研药物的开发工作,以及Roivant专有技术平台DrugOme和Digital Innovation的使用权。
贺建奎事件一年后
2018年11月,南方科技大学原副教授贺建奎声称,其利用CRISPR-Cas9基因编辑技术改变了7对夫妇的胚胎DNA,并创造出全球首例免疫艾滋病基因编辑双胞胎,引发基因编辑伦理丑闻。 对此,2019年3月13日,包括张峰、Emmanuelle Charpentier在内的7个国家的18位领先研究人员和生物伦理学家在《Nature》杂志上发表文章《Adopt a moratorium on heritable genome editing》,呼吁在全球范围内暂停人类生殖系基因编辑的所有临床用途。同时他们还表示:“‘全球暂停’并不意味着永久禁止。相反,我们呼吁建立一个国际框架,在这个框架中,各国在保留自己决定权的同时,自愿承诺除非满足某些条件,否则不予批准任何临床生殖系的基因编辑试验。” 2019年12月30日,据新华社报道,“基因编辑婴儿”案在深圳市南山区人民法院一审公开宣判。贺建奎、张仁礼、覃金洲等3名被告人因共同非法实施以生殖为目的的人类胚胎基因编辑和生殖医疗活动,构成非法行医罪,分别被依法追究刑事责任。
全球首款埃博拉疫苗获批
2019年11月11日,欧盟委员会(EC)批准默沙东(Merck & Co)的埃博拉疫苗Ervebo(V920)上市,成为全球首款获批上市的埃博拉疫苗。12月19日, FDA同样宣布批准Ervebo上市,成为了FDA批准的首款用于18岁及以上人群的主动免疫,以预防扎伊尔型埃博拉病毒(Ebola Zaire)引起的埃博拉病毒病(EVD)。 2018年8月以来,刚果民主共和国爆发了该地区有史以来第二大的埃博拉疫情,在此期间约有2000多人死于该疾病。在该疫苗获批之前,默沙东便为该地区提供了该疫苗的大量研究制剂,并完成了超25万人次的疫苗接种。
此外,强生旗下的杨森制药公司也正在开发另外一种埃博拉疫苗,该疫苗目前已给予刚果东部戈马市中的5万人使用。与默克1针疫苗方案相比,强生疫苗需要在首针注射8周后,进行再次注射。该疫苗目前已向欧洲药品管理局(EMA)提交了2份营销授权申请(MAA)。
普渡制药申请破产
曾经以阿片类止痛药OxyContin(奥施康定)闻名的普渡制药(Purdue Pharma),因深陷数千起与阿片类药物成瘾危机有关的诉讼,并无力支付100-120亿美元的法律和解费用,从而申请破产。当地政府公开指责了该公司因过度积极推销处方止痛药OxyContin,并在该产品的过量风险提示上误导医生和患者,进而助长了美国阿片类药物危机。截止目前美国社会已有数千人因阿片类药物过量服用而死亡。在普渡制药申请破产的同时,其资产将被重组为一家新的公司,且新公司的董事会将由债权人选出,由破产法院批准。根据声明,这家新公司将以几乎0成本的方式来生产治疗阿片成瘾的相关药物,例如纳美芬和纳洛酮。
致癌物召回年
因出现问题而召回药物的情况在历史上并不少见。而2019年的较多药物召回事件似乎都与制药工艺过程中存在致癌物质有关。自2018年华海药业的缬沙坦事件后,FDA一直在针对高血压和心衰药品(称为ARB)中的NDMA(N-亚硝基二甲胺)和其他亚硝酸胺类杂质进行调查,并建议召回了许多制造商的多种类型的血管紧张素II受体阻滞剂产品。 直到2019年9月13日,FDA、EMA发文表示:不仅仅是降压药物受到污染,相关雷尼替丁药品(一种抑制胃酸分泌的药物,可用于治疗消化性溃疡等疾病的经典治疗药物。)中也含有低水平亚硝胺杂质NDMA。于是,雷尼替丁的召回风波开启了。
在美国FDA发出安全警告后,陆续有多家跨国药企自愿召回产品并遭受冲击。先是诺华宣布暂停山德士公司在市场销售所有含有雷尼替丁的药物,包括在美销售的胶囊药物,涉及26个国家。GSK也宣布,暂停向包括印度在内的全球市场供应雷尼替丁药物,并启动召回,以作为预防措施,以待全球正在进行的测试和调查得出结果。其他药企诸如印度瑞迪博士药厂、山德士公司、加拿大Apotex制药公司、印度Strides制药陆续表示,暂停其雷尼替丁药物在全球或美国的供应或销售、自愿召回美国境内相关批次、某些规格、相关供应原料生产的雷尼替丁。
HIV治疗的持续改善
2018年11月,雅培实验室的研究人员发现了一种新的HIV毒株,这也是近20年来首次发现的一种新的HIV-1亚型,它的起源可以追溯至非洲的刚果民主共和国。这一新菌株的发现,意味着研究人员或可开发出针对艾滋病的潜在新疗法。
自艾滋病在全球流行以来,已有超过7500万人曾被HIV病毒感染。这一曾经近似“死刑”宣判的疾病,随着新药物和新疗法的发展,已有超3790万人得以控制病情并继续存活下来。
除此之外,今年还有很多针对HIV病毒的新疗法获批。例如,默沙东Pifeltro和Delstrigo被批准联合用药治疗HIV-1患者;吉利德公司的Descovy被批准用于HIV暴露前预防。此外,还有许多新的疗法尚在研发之中,例如,GSK旗下ViiV的Cabotegravir和杨森的rilpivirine联合用药;北京大学邓宏魁教授及其团队发明的使用CRISPR技术和调节蛋白BRD4的骨髓移植;长非编码RNA的遗传修饰等等。
随着2019年这些潜在疗法的发现,将为未来HIV患者的治疗带来更多的选择。
全球首颗3D仿生心脏
近年来,3D打印技术逐渐成熟。2019年4月,特拉维夫大学的研究人员使用患者自己的细胞及各种生物材料成功地打印了第一颗含有血管的3D仿生心脏。 领导该研究的Tal Dvir教授表示:“这颗心脏是由患者的细胞和特定的生物材料制成的。在我们的工艺过程中,这些材料可作为生物墨水(由糖和蛋白质制成的物质),用于复杂组织模型的3D打印。过去人们设法对心脏结构进行3D打印,然而无法打印出相应的细胞或血管。我们的研究结果证明了未来设计出可替代的个性化组织和器官的潜力。” 这也将意味着,人类已在3D打印器官方面取得重大突破,其发展方向不仅是为了科学研究,也可能是为了器官替代。
(编辑:李国坚)




 扫码下载智通APP
扫码下载智通APP