专访泰格医药(03347)曹晓春:CRO并购与全球化之路如何走?
本文来自微信公众号“生辉”。
今年 8 月初,泰格医药(03347)在港交所主板挂牌上市,成为继药明康德(02359)、康龙化成(03759)后,第三家在 “A+H” 两地上市的 CRO 公司,市值近千亿港元。
CRO(Contract Research Organization)即合同研究组织,可分为临床前研究 CRO 和临床研究 CRO。简单的说,临床前研究 CRO 主要是协助客户做药物研发;临床研究 CRO 主要是提供临床试验服务。
作为一家专注于为新药研发提供临床试验全过程服务的 CRO,自 2004 年成立以来,泰格医药逐步建立起了从药物研发到临床试验等完整的生物制药研发服务体系,其业务范围主要为客户提供临床试验技术服务、临床试验相关及实验室服务。
泰格医药联合创始人、执行董事、总经理曹晓春拥有近 25 年生物医药研发、注册和临床研究经验,以及超过 15 年的企业管理经验。关于泰格医药近年来快速发展的 “秘密” 和港股上市后的计划,生辉与曹晓春女士进行了对话。
关键词之“创新”
生辉:创新药企业逐渐成为泰格医药的重要客户结构之一,如何看待客户结构的变化?面对客户结构的变化,泰格医药采取了哪些应对措施?
曹晓春:在 2015 年之前,国内的创新药企业相对较少。2015 年之后,为了促进医药创新,中国出台了众多鼓励措施,并不断深化审评审批制度改革。中国的制药产业的重心也逐渐从仿制药转变为创新药。再加上中国自身研发能力的提升,资本市场的助力,涌现出了非常多中国本土的优质创新药企业。泰格医药作为一家提供临床试验全过程专业服务的 CRO,我们也看准时机,承接了大量本土创新药项目,把握住了快速发展的机遇。
2017 年,中国加入 ICH(编者注:人用药品注册技术规定国际协调会议,目的是为药品研究开发、审批上市等制定统一的国际性指导标准)以后,临床开发也加速与国际接轨,比如海外临床数据也可以作为补充数据,支持在中国上市申请,吸引越来越多的全球生物制药公司将创新药物引入中国市场,并在中国进行国际多中心临床研究。
泰格医药很早就建立了一套 ICH-GCP 标准的质量管理体系,以保证项目执行的质量。与此同时,我们也在产业链的延伸和区域服务能力上持续投入,打造完整的药品和医疗器械临床研究一体化、全方位的研发服务平台。
生辉:在泰格医药服务的客户中,创新药企业和传统仿制药企业所需服务的主要差别是什么?
曹晓春:在创新药还未兴起时,中国医药市场主要是仿制药。在仿制药企业的服务中,相对来说“有据可依”。因为仿制药在国外已经上市,有很多资料可以查阅。在临床过程中可能有哪些风险、如何更好的设计方案等,我们比较清楚,有据可依。
在创新药企业的服务中,需要的专业度更高。因为在项目进行过程可能会随时出现一些没有预料到的问题,例如临床试验中病人出现的各种反应。我们需要根据不同的情况,及时做出研发策略或临床研究方案的调整和完善。研发策略或临床研究方案对于项目的成败非常关键。一个好的策略可以避免走弯路,对产品的顺利开发很重要。基于我们丰富的经验积累,对于可能发生的风险及应对措施都更具备专业性,这也是很多创新药企业都愿意与我们合作的原因。
生辉:在临床试验中,泰格医药如何进行招募?
曹晓春:在临床试验中患者招募是难点,尤其是在国外市场。因为海外各地人口少,同一疾病的病例也很少,所以成本就很高。当然,国内的临床试验招募也并不容易。而我们有着一支经验丰富的患者招募团队,可以帮助申办方招募患者或者建库志愿者。
在患者招募方面,泰格医药主要通过两种方式:一种是医院内渠道,一种是医院外渠道。在医院内的招募,我们的临床试验现场管理团队会以医生助理的身份进入到医院中,协助医生管理患者。在这个过程中,我们会接触到很多病人,根据项目筛选条件进行筛选后推荐到项目中。在医院外的招募,我们会通过社区、多媒体渠道等方式寻找合适的病人,并将其推荐到项目中。在此过程中我们都会严格遵守方案、GCP(Good Clinical Practice,药品临床试验管理规范)和伦理要求。
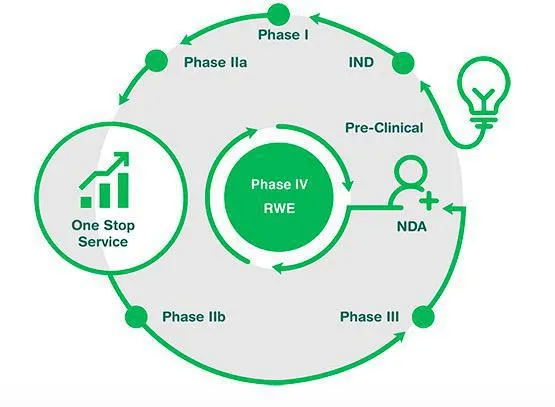
图 | 泰格医药所提供服务流程图 (来源:泰格医药官网)
生辉:如何看待国内外在生物制药行业的发展情况,有哪些差异?这些差异在泰格的业务表现上有哪些体现?
曹晓春:在生物制药领域,国外的发展比中国早了 30 到 40 年,所以他们相对比较成熟。现在很多大跨国药企在研发投入方面非常大,他们的研发体系也很完善,对于研发的风险控制和成本控制方面会更灵活。
制药企业对于 CRO 的需求大概会经历三个发展阶段。
在第一阶段时,制药企业团队的组建才刚刚开始,研发体系还不太完善,所以很需要 CRO 给他们提供一些基础知识和经验,弥补人员的不足,帮助他们进行研发。中国的创新医药企业很多还处于第一阶段;
在第二阶段,部分制药企业自己建立了完整的研发团队,研发体系逐渐完善,对 CRO 的需求相对会减少;
在第三阶段,就像现在很多国际大药企,他们对 CRO 的需求又逐渐增多,因为他们对风险或成本等因素的考虑会更多,会更灵活地使用 CRO 所提供的服务。
中国的创新药起步比欧美晚,但发展非常迅速。当前药物研发全球化趋势不断加强,中国也成为了全球重要的市场,中国的临床试验数量由 2015 年的 339 项增加到 2019 年的 1031 项,在中国进行的国际多中心临床试验数量也在逐步增加。我们也通过不断完善临床研究运营体系、深度布局临床研究网络、积极并购、自建团队等方式强化我们的运营和服务能力,以满足客户全球化同步开发的需求。
关键词之“并购”
生辉:近年来,泰格医药完成了不少项目的并购。并购对于泰格医药的意义是什么?在选择并购项目时会考虑哪些因素?
曹晓春:成功的并购是泰格医药的优势之一。通过战略收购,我们能不断地完善和丰富我们的研发服务能力,同时拓展服务的地域范围。
我们选择并购项目时,主要会从 3 个方面考虑:
第一个,可以补全我们的临床研究服务链条。我们并购的一些企业,相对来说是比较有特色的,在某一领域做得比较好的,这样的公司可以加强我们的服务能力。比如 2014 年我们收购了方达,以提升我们的实验室服务能力;2017 年我们收购捷通,增强了我们的医疗器械研发服务能力。
第二个,区域的布局。例如,2015 年我们收购了韩国最大的临床 CRO 之一的 DreamCIS,以强化我们在韩国的服务能力。目前我们正在进行全球化发展,也计划并购一家有全球化布局的公司。
第三个,公司本身具备运营能力。我们更希望并购有完整团队、具备运营能力的公司,这样的公司整合起来相对容易。当然,和我们理念共通也很重要。
生辉:7 月 20 日德琪医药宣布完成 9700 万 C 轮融资,而泰格投资早在 2017 年就对这家公司进行了 A 轮投资,主要看中的是德琪医药的哪些方面?接下来泰格投资是否会有新的投资计划,主要看好哪些赛道?
曹晓春:成功的投资也是泰格医药的优势之一。德琪医药拥有非常专业的研发和管理团队,丰富的研发管线,其创始人、董事长兼 CEO 梅建明博士也曾在多个大型跨国制药公司担任重要职位,负责了多个创新药物的研发工作。我们非常看好德琪医药未来的发展。
除了主营业务外,我们也对优秀的创新生物制药公司进行少数股权投资,建立长期合作关系,打造行业生态圈。我们主要看创新生物技术和医疗器械行业,在投资时主要关注处于早期研发阶段的创新项目,并通过我们广泛的行业网络和对于新药开发的专业支持,进行分析和评估。
生辉:此前我们曾经和业内人士交流,对方认为对于 CRO/CDMO 企业而言,业务在精而不在多,在某种业务上拥有独特性优势要比全链条布局更重要,你如何看待这种观点?泰格的思路又是什么?
曹晓春:我觉得这要分阶段去看,如果一家公司在起步阶段,一定要把一块业务做好、做精,这样才有竞争力。任何一个行业、任何一家公司都是一样的,如果要在这个市场里竞争,那就要把自己的业务做好。当公司发展到一定阶段,能够做好一个业务的前提之下,有余力就可以向下一个业务板块进军。当然,每一家公司都有着自己的发展和增长策略。对于泰格来说,我们要求自己每块业务都要做到最强、最好,给客户提供全方位的服务。
关键词之“全球化”
生辉:泰格医药是继药明康德、康龙化成之后,第三家实现 “A+H” 股的 CRO 公司,为何选择在港股二次上市?
曹晓春:对于泰格医药来说,境外资本平台有利于在海外获得融资渠道,不断丰富和增强我们的新药研发服务能力。此外,境外上市能更好的满足国际化投资人的需求,也可以为公司并购提供更多的工具的选择。在境外主流的证券交易所上市,能够进一步提升公司国际化的品牌价值,为业务上带来更好的商业机会。我们将以港股上市作为“新起点”,完善全球化布局和运营能力,提升新药研发服务能力和效率,助力全球生物医药创新企业加快产品市场化进程。
生辉:泰格医药登陆港交所之后的下一步计划是什么?
曹晓春:成功在香港上市,不仅为我们未来全球化经营和业务拓展提供了强有力的资本支持,加快国际化战略的推进步伐,也为我们服务全球创新药开发打下坚实基础。
对于香港上市的募集资金,我们将主要用于扩大和提升临床试验技术服务和临床试验相关服务的种类及能力、为潜在收购和少数股权投资提供资金、开发先进技术以进一步提升综合服务能力的质量和效率、补充运营资金等。
对于未来发展,首先我们将继续加强我们的服务能力,丰富我们的服务种类,满足客户的多元化需求。其次,继续推进我们的国际化战略,加快全球化的布局,提升在主要医药研发市场的服务能力,这也是我们募集资金的主要投入方向。第三,加大在创新技术方面的投入,探索跨行业合作,实现协同效应,为客户提供更多创新解决方案。第四,我们会继续深化与客户的合作,进一步扩大客户群。第五,人才是 CRO 的重要资源,我们也将继续吸引、培养和留住优秀的临床研究人才。
生辉:泰格医药如何做老客户的留存和新客户的开发?
曹晓春:对于老客户来说,最重要的还是看项目做的好不好。良好的沟通和专业的服务,是维系客户关系的基础。我们每周会有给客户的周报,也会有跟客户沟通的项目会,客户也会经常和我们一起去医院跟进项目进度,我们跟客户是一个共同的团队。把项目做到客户满意和放心,老客户的留存自然会很好。
对于新客户来说,更重要的是口碑。其实生物制药领域圈子挺小的,虽然现在生物医药企业很多,但创业者很多是同一个公司、同一个学校或是同一个地区出来的,彼此都认识。所以我们新客户的拓展更多的是靠老客户的推荐和我们在行业内的口碑。
生辉:从今年 5 月开始,泰格医药多次进入深交所外资持股预警名单,主要原因是什么?如何看待外资对 A 股部分公司的“狂热”?
曹晓春:外资对于部分 A 股公司的认可,主要是看中了中国未来发展的巨大潜力。增持泰格医药,也表现出了资本市场对于泰格医药未来发展的看好,以及对中国生物医药产业和监管的认可。
生辉:在 CRO 行业,国内外公司有哪些差异?在化学药逐渐转向生物药的趋势中,CRO/CDMO 需要作出哪些改变?
曹晓春:中国的 CRO 行业整体起步较晚,相对于美国的临床 CRO 市场来说,中国的临床 CRO 市场目前尚处于早期阶段。根据统计,2019 年美国的临床 CRO 市场规模是 209 亿美元,预计 2024 年会达到 307 亿美元,复合年增长率为 8%。而中国的临床 CRO 市场规模 2019 年为 37 亿美元,预计 2024 年可以达到 137 亿美元,复合增长率可以达到 30%。
中国的临床 CRO 市场增长非常迅速,这得益于对于创新药物的投资不断增加,监管制度日趋严格,对于符合国际质量标准的 CRO 的需求不断上升。此外,中国患者人群规模大,还存在着大量未被满足的临床需求,这些都推动了中国临床 CRO 和新药研发的快速增长。
行业的发展也对 CRO 公司提出了更高的要求。比如药物研发的外包渗透率上升,具备专业知识和经验丰富的人才团队的临床 CRO 将更具优势,可以帮助客户处理更为复杂和具有挑战性的临床开发计划。
其次,随着监管的日趋严格和客户需求的多元化,具备向客户提供综合多元化服务的能力将会越来越重要。
第三,在全球化的大环境下,越来越多的生物制药和医疗器械公司趋向于进行全球同步开发,因而需要临床 CRO 协助其开展和管理海外进行的临床试验或者国际多中心临床试验。
第四,数字化、大数据和更多先进技术的采用。临床 CRO 的数字化水平将会持续提升,也将越来越采用更多先进技术,协助客户处理更多复杂且新颖的难题,开发更多创新疗法。比如基因和细胞治疗研发增加,也将需要我们不断开发新技术,用于支持临床开发,提升研发效率。
(编辑:李国坚)




 扫码下载智通APP
扫码下载智通APP