2021医保目录初审名单!首款CAR-T、首款国产ADC、多款“天价药”悉数在列!共271款!
7月30日,医保局公布2021年国家医保药品目录调整通过初步形式审查药品名单。
本次名单包含三种类型药品:符合条件1(2016年1月1日至2021年6月30日期间,经国家药监部门批准上市的新通用名药品)的新通用名药品共160个,其中中成药新药仅有6种;条件2(2016年1月1日至2021年6月30日期间,经国家药监部门批准,适应症或功能主治发生重大变化的药品)新增适应证药品13种;条件4(纳入《国家基本药物目录(2018年版)》的药品)来自基药目录的品种仅有6个。
国家医保局在公示工作解读中表示,通过初步形式审查的药品“代表经审核该药品符合相应的申报条件,初步获得了参加下一步评审的资格。”2021年7月1日9时至2021年7月14日17时,共收到企业申报信息501条,涉及药品474个。经审核,271个药品通过初步形式审查。通过初步形式审查的目录外药品中,2016年以后新上市的药品占93.02%。
这271个的药品所涉及的企业将在2021年医保谈判中展开竞争。
从具体品种来看,PD-1/PD-L1的竞争越来越激烈,四个获批了新适应证的国产PD-1产品全部进入初审名单,君实特瑞普利单抗注射液新增2个适应证、百济替雷利珠单抗注射液新增3个适应证、信达的信迪利单抗注射液新增3个适应证、恒瑞注射用卡瑞利珠单抗新增2个适应证。
跨国药企一边,阿斯利康(AZN.US)的度伐利尤单抗(PD-L1)、百时美施贵宝(BMY.US)的纳武利尤单抗、默沙东(MRK.US)的帕博利珠单抗也均进入初审名单。只有罗氏的阿替利珠单抗(PD-L1)未出现在名单中,这也几乎宣告着T药将再次无缘医保。
PARP抑制剂方面,2021年谈判药品涵盖期间国内共上市了4个产品,谈判压力的陡增。
此前谈判中仅有阿斯利康的奥拉帕利上市,并最终通过2019年医保谈判进入医保。而此次初步审查中两个新上市产品恒瑞医药的氟唑帕利、百济神州(06160)的帕米帕利均通过申报进入,阿斯利康的奥拉帕利新增适应证和再鼎医药尼拉帕利的新增适应证也进入形式审查。
EGFR抑制剂同样迎新上市药品,竞争激烈。今年3月,艾力斯上市了伏美替尼,用于治疗EGFR T790M突变阳性的局部晚期或转移性非小细胞肺癌(NSCLC)。同类型药品中还有AZ的奥希替尼新获批适应证进入初审名单,豪森的阿美替尼在去年进入医保,今年暂时没有新获批适应证进入。此外在非小细胞肺癌治疗药上,贝达药业恩沙替尼(ALK靶点)也获批用于治疗NSCLC。
曾经备受争议的绿谷制药阿尔茨海默病新药“九期一”再次进入了此次初审名单中,目前“九期一”价格为895元/盒,这次是否会进入医保呢?此前“九期一”刚刚上市时就迎来了市场的疯狂抢购,如被纳入或将为其销量带来进一步的增长。
几乎所有Biotech在第一时间将旗下新获批产品送进了初审名单。譬如荣昌生物旗下两款产品,泰它西普和注射用维迪西妥单抗,后者为首个国产ADC产品,于6月获批用于至少接受过2种系统化疗的HER2过表达局部晚期或转移性胃癌(包括胃食管结合部腺癌)患者的治疗。
特别值得关注还有本次初步形式名单中的一些昂贵新药。譬如复星凯特的阿基仑赛注射液,这是中国首个获批的CAR-T产品,有消息称目前治疗费用约为120万元;还有之前的诺西那生钠注射液,去年未进入医保谈判也未被纳入,目前在国内该药售价为每支55万元,属于自费药物,曾创下了中国药品售价的纪录。
针对这些“天价药”能否进入目录,国家医保局在公示工作解读中特别进行了解释:“一些价格较为昂贵药品通过了初步形式审查,仅表示经初步审核该药品符合申报条件,获得了进入下一个调整环节的资格。这类药品最终能否进入国家医保药品目录,还要接受包括经济性等方面的严格评审,独家药品还要经过价格谈判,谈判成功的才能进入目录。”这些高昂的药品最终能否纳入医保将成为今年医保谈判的一大看点。
国家医保局表示初步形式审查的药品及资料进行公示结束后,将按程序处理公示期间收到的反馈意见和建议,确定最终通过形式审查的药品范围。同时,按照《工作方案》要求,组织开展专家评审等后续工作。
以下为2021年国家医保药品目录调整通过初步形式审查的申报药品名单:
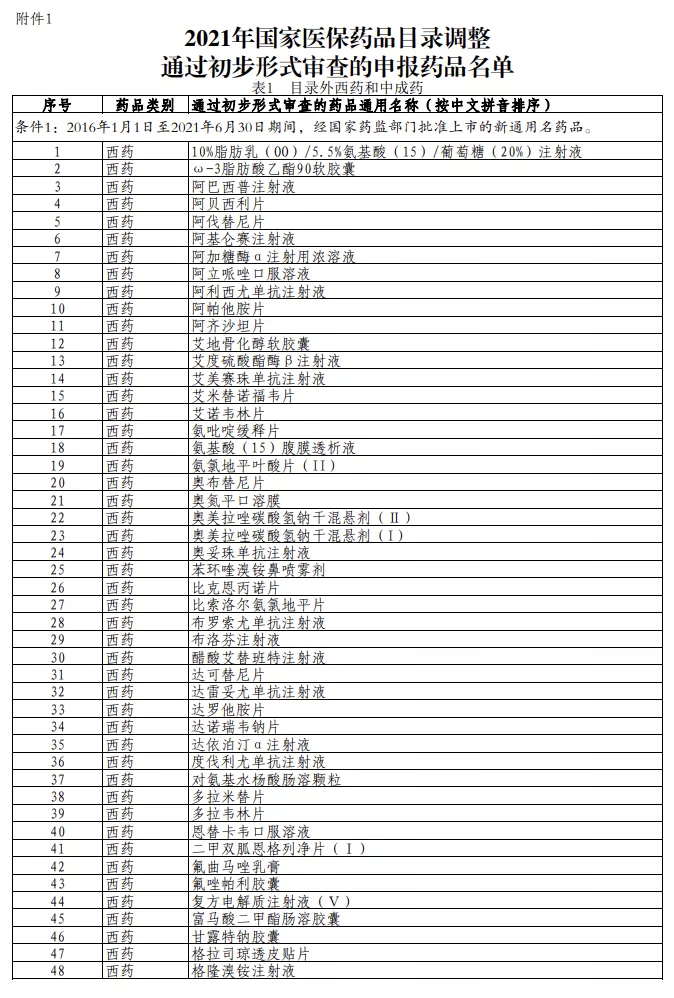
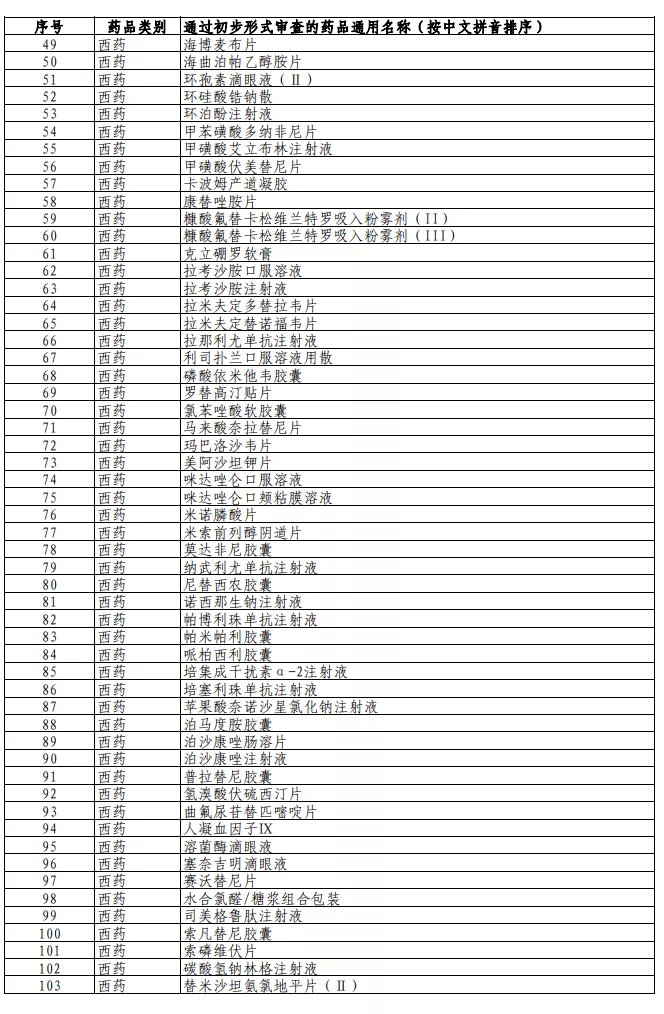
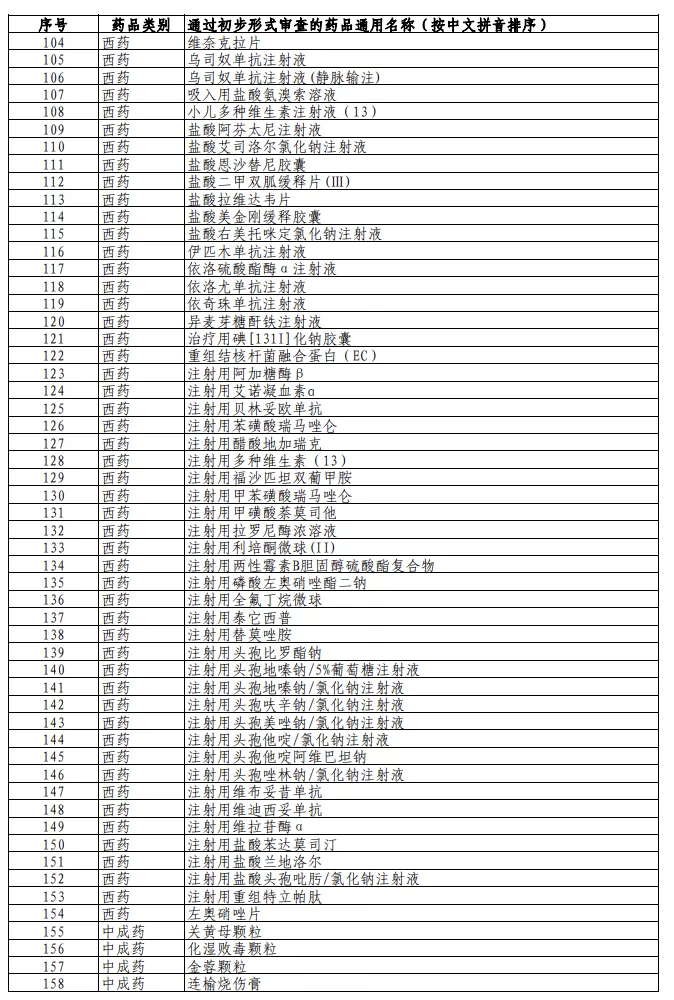
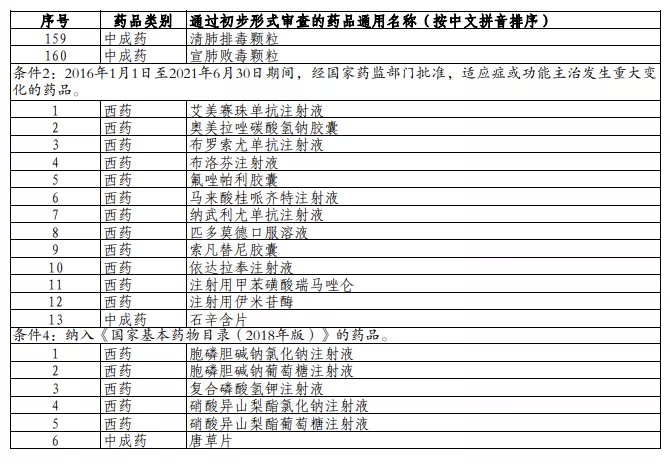
本文选编自“E药经理人”,智通财经编辑:秦志洲




 扫码下载智通APP
扫码下载智通APP