VV116未能激起资本巨浪,君实生物(01877)能否赢下竞速赛?
今年2月份,辉瑞新冠口服药Paxlovid在国内应急附条件获批。这款口服特效药的特点在于,能让新冠症状出现后3天内开始治疗的患者住院和死亡风险降低89%。
出色的有效性数据让Paxlovid在去年12月立马获得FDA的紧急使用授权(EUA)。2个月后,Paxlovid顺利进入国内并被纳入医保,用于治疗成人伴有进展为重症高风险因素的至中度新冠患者。
不过,Paxlovid并未像市场想象的那样在国内顺利铺开覆盖。一方面原因在于,国内整体疫情控制良好,中度及重度患者较少;还有另一方面原因就是,即便Paxlovid进入医保,其单盒售价也高达2300元,以至于市场上甚至传出“Paxlovid要榨干医保”的说法。
庞大的潜在市场、不受欢迎的市场竞品,多重因素杂糅下,国产新冠特效药的前景似乎很明朗。
首款国产新冠特效药上市时间表确定?
前段时间,一则消息在医药圈疯传:“目前君实生物(01877)VV116与辉瑞Paxlovid在瑞金医院的头对头临床试验已入组完成,预期15号左右出中期数据,5月底6月初获批上市”。
智通财经APP了解到,君实生物VV116是市场上非常关注的有望成为国内首款新冠口服特效药的产品之一,其临床及上市进展上国内医药圈热搜自然是很正常。
5月11日,网上流传的一则“上海瑞金医院的副主任医师交流纪要”显示,君实生物的临床进展,改良版的瑞德西韦,4月第二周在上海开始入组,4月底入组完成,达到800多人,分为Paxlovid药组和VV116组,各400人左右,观察主要临床终点为转阴时间长度,次要终点为转重症比例。目前基本完成给药。
在这则利好消息刺激下,5月12日,君实生物-U(688180)科创板收涨9.99%。以上临床数据无疑是近段时间以来关于VV116的“主菜”了。不过在“主菜”前,还有一道“前菜”。
5月18日,VV116在中国奥密克戎感染受试者中首个小样本量临床研究正式发布,相关成果发表在Emerging Microbes&Infections杂志。
智通财经APP了解到,这是一项开放性、前瞻性队列研究,用于评估VV116对非重症奥密克戎感染患者核酸转阴时间的影响。
此次参与研究的受试者为今年3月8日-24日区间感染SARS-CoV-2 Omicron变异体的国内患者,总共136名。其中治疗组60例接受VV116治疗(300mg,BID×5天),对照组76例除标准治疗外未接受VV116治疗。
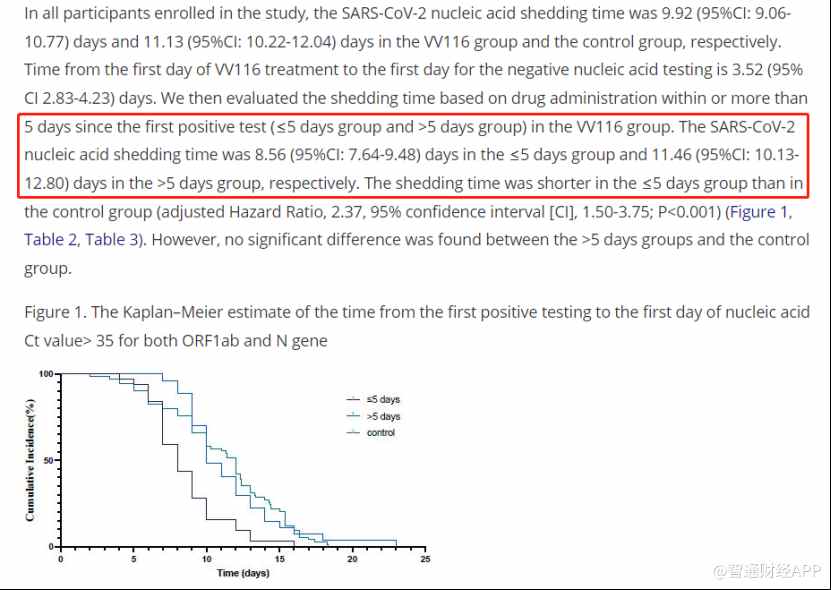
研究数据显示,从患者首次检测阳性到首次VV116给药的中位时间为5天(用药时间范围:2-10天)。并且首测阳性的5天内接受VV116治疗的患者,其核酸转阴时间比对照组短(8.56天vs 11.13天)。
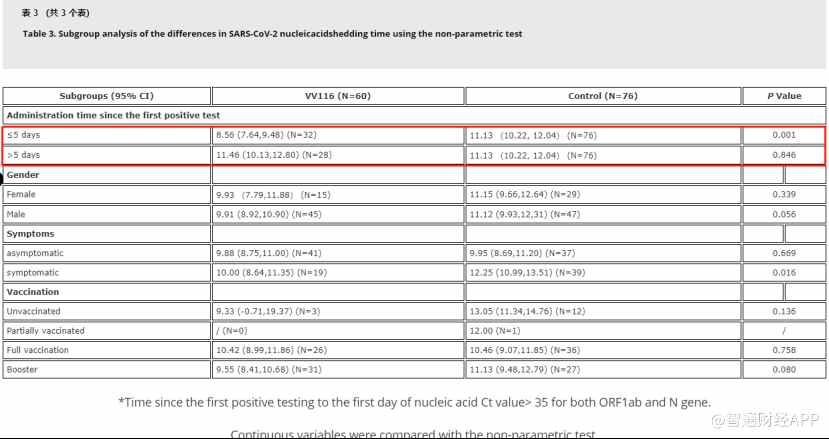
值得一提的是,针对核酸转阴时间的亚组分析结果显示,患者在首次检测阳性后10日内服用VV116均有效果,5日内服用药物疗效则更佳,且无性别差异。在有症状的亚组分析中,VV116组患者核酸转阴时间比对照组短(P=0.016),但VV116对无症状感染者无显著差异。
在安全性方面,数据显示,VV116组共出现了9例不良反应事件,其中并无严重不良反应事件。
虽然此次数据在一定程度验证了VV116拥有可观的有效性和安全性,但该篇研究报告依然提到,由于其所纳入的样本量有限,所有受试者均未发展为重症或危重症,因此该项研究未能收集到足够多的数据进一步分析VV116是否对于奥密克戎感染重症化具有预防作用,仅初步评价了轻症患者中核酸转阴这单一指标。
而这也是此次数据被不少业内人士“吐槽”的一点。样本量有限,基线平衡便相较大样本量状态更难做。以此次研究为例,对照组在高血压、有症状患者数量以及未接种疫苗患者数量等基线特征上,与治疗组差距较大。
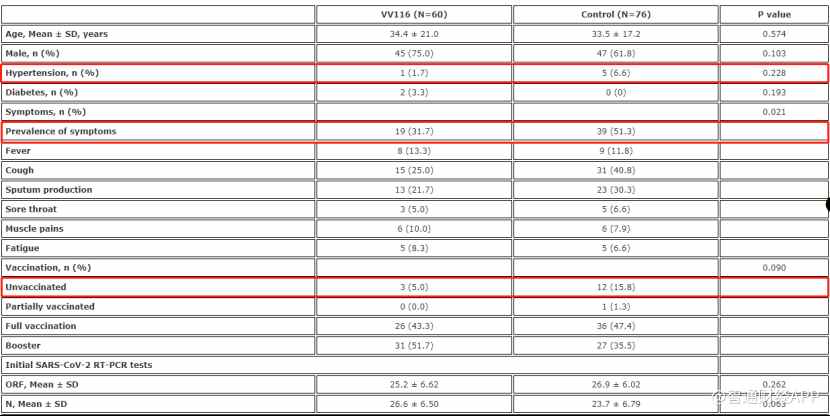
从严谨的角度考虑,从这个基线平衡下得出的平均转阴时间(8.56 vs 11.13)结论,或不足以完全证明治疗组和对照组在基线平衡更好的大样本量临床下的差异情况。
另外,对比此前披露的Paxlovid的国内真实世界研究数据,同样是小样本量的临床研究,Paxlovid治疗组的基线特征数据中,未接种疫苗的患者比例为25%,全面接种患者比例为17%,与此次VV116对应的5%和43.3%同样存在较大差异,因此这两次临床研究数据无法进行对比。
可见,此次披露的临床数据,虽在一定程度验证了VV116的有效性和安全性,但并不能完全满足市场对于其最终疗效以及与竞品对比的期望。因此5月18日,君实生物在科创板收跌2.82%,港股也仅收涨不到2.5%。
所以,对于市场而言,“前菜”仅仅只是“前菜”,至于所谓的首款国产新冠特效药上市时间,或许还要比我们想象的晚一些。
国产新冠特效药“好饭不嫌晚”
虽然相比于此前VV16“将在5月中旬出中期数据,月底上市”的传闻,现实进度可能稍晚一些,并且首款国产新冠特效药的桂冠最终花落谁家也不得而知,但对于市场来说,正在“竞速上市”的三款国产新冠特效药谁先上市都是极大利好,因为这一赛道的增长潜力巨大,拥有可观的回报预期。
之所以市场能得出以上结论,在于国产新冠特效药在上市后需求量大,产业链价值丰富。
目前来看,“新冠疫苗预防+特效药治疗”是应对新冠疫情最有效的防治策略。面对不断出现的新型变异毒株,疫苗保护效力有限,中和抗体也存在随着突变的发生而失去中和效力的风险。
相比之下,以新冠病毒保守结构域为靶点的小分子药物受毒株变异的影响较小,加之生产成本低、服用方便等优势,其或将成为后续国内防疫实现动态清零的关键战略资源。
据东吴证券预测,参照2009年甲型H1N1流感期间国家药品储备以及WHO的流感大流行预案中的推荐方案,我们预计国内新冠药有望储备1-3亿人份/年。
对于VV116来说,参照其在乌兹别克斯坦定价,我们预计国内一人份定价可能在600-1000元。审慎预测下,国内VV116销售额约为600-1000亿元,乐观预测下,销售额有望达到1800-3000亿元。
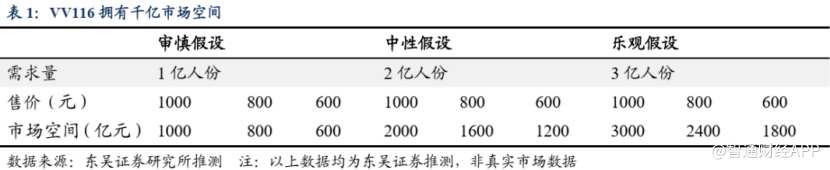
除此之外,VV116相对辉瑞Paxlovid还存在一个优势在于,君实VV116为一款中轻症新冠特效药,相较于Paxlovid针对中重症来说,VV116能作为战略常备药,具有显著的销售确定性,在国内销售更具优势。所以这个时间点,投资者还是需要静待VV116在5月底或6月初揭盲,届时整个国产新冠特效药赛道或许都会按下加速键。




 扫码下载智通APP
扫码下载智通APP