4项重磅临床数据入选ASH口头报告,亚盛医药-B(06855)近2个月股价涨逾80%价值凸显
11月4日早盘,亚盛医药-B(06855)股价跳空高开,最高达到20.3港元,涨幅达到18%。在连续三个交易日上涨后,亚盛医药股价也来到了近4个月来的新高。近2个月,公司股价区间最高涨幅达到80.6%。
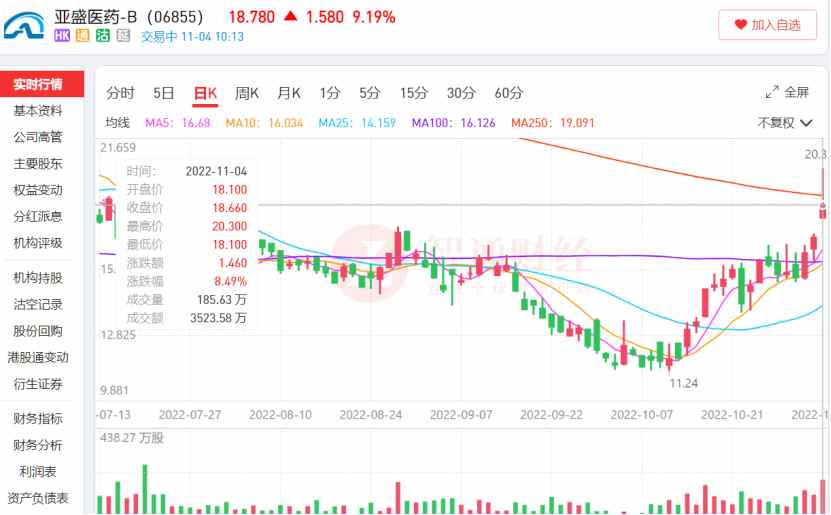
市场之所以有如此积极的反馈,在于前一日亚盛医药宣布,公司向第64届美国血液学会(American Society of Hematology,ASH)年会递交的4项临床阶段研究数据全部入选口头报告,全球创新实力再获验证。
一年一度的ASH年会是全球血液学领域规模最大的国际学术盛会之一,全面涵盖了血液疾病的病因研究和治疗研究。第64届ASH年会将于2022年12月11日至14日在美国新奥尔良以线下结合线上的形式举行。
今年,亚盛医药核心品种、首个商业化产品、原创1类新药奥雷巴替尼(商品名:耐立克®)共有3项临床进展获选年会口头报告。
这是该品种的临床进展连续第五年入选ASH年会口头报告,五连冠的佳绩充分体现国际血液学界对其疗效和安全性的认可,也体现出奥雷巴替尼的创新含金量以及亚盛硬核的研发实力。
值得一提的是,耐立克®在美国慢性髓细胞白血病(CML)和费城染色体阳性急性淋巴细胞白血病(Ph+ ALL)患者中的有效性和安全性数据为亚盛医药首次公布,且一经公布即入选口头报告。
数据显示,耐立克®在难治性CML和Ph+ ALL患者中的有效性和耐受性良好,即使在ponatinib或asciminib耐药的患者中,亦显现出很强的疗效。这表明耐立克®有望成为全球首个能有效克服ponatinib或asciminib耐药的新一代BCR-ABL抑制剂。
耐立克®另外两项入选口头报告的研究分别为其治疗T315I突变耐药CML患者的关键II期注册临床研究的最新数据,和其用于中国CML耐药患者的5年长期随访数据(I期临床研究),进一步验证安全性和有效性。去年,耐立克®就是凭借关键II期注册临床研究的数据斩获上市,成为中国首个且唯一获批上市的治疗携T315I突变耐药慢性髓细胞白血病的药物,充分体现了本土创新、全球领先。
同时,公司细胞凋亡管线重要品种Bcl-2选择性抑制剂APG-2575单药或联合治疗初治、复发或难治(R/R)慢性淋巴细胞白血病/小淋巴细胞淋巴瘤(CLL/SLL)患者的全球II期临床研究初步数据也成功获选ASH年会口头报告。该数据也是公司首次披露,备受国际业界和市场双重期待。
作为全球第二个、国内首个看到明确疗效、并进入关键注册临床阶段的Bcl-2抑制剂,APG-2575在此次ASH年会口头报告的数据体现了该品种在R/R CLL/SLL患者中强劲的单药和联合治疗潜力。
数据显示:APG-2575联合acalabrutinib治疗R/R CLL/SLL的客观缓解率(ORR)达98%;APG-2575联合利妥昔单抗治疗的ORR达87%。此外, 单药治疗的研究结果和前期临床研究结果相似,再次展现了APG-2575优秀的疗效和安全性;而联合治疗的研究,特别是和acalabrutinib的联合治疗的研究结果,显示了超高的有效率。同时在肿瘤溶解综合征(TLS)的发生率和血液学不良事件等方面,联合治疗也保持了与APG-2575单药治疗相当的出色安全性。
亚盛医药首席医学官翟一帆博士表示:“今年,亚盛医药共有四项临床数据入选ASH年会口头报告,可谓是大丰收,我们对此感到非常激动。
其中,耐立克®共获三个ASH年会口头报告,创下了‘五连冠’的新历史,这是国际血液学界对该品种的巨大认可。此次亚盛医药首次公布的耐立克®海外研究数据表明,该品种有望成为全球首个能有效克服ponatinib和asciminib耐药的BCR-ABL抑制剂。这意味着耐立克®有潜力进一步解决全球CML患者急需、改变全球CML治疗格局,这让我们无比振奋。
此外,APG-2575取得的成绩也非常亮眼。APG-2575是首个在中国进入临床阶段的、本土研发的Bcl-2抑制剂,也是全球第二个、国内首个看到明确疗效、并进入关键注册临床阶段的Bcl-2抑制剂。此前,亚盛医药多次公布了该品种单药治疗R/R CLL/SLL患者的积极数据,获业界认可和关注。
Bcl-2抑制剂与BTK抑制剂的联合治疗前景一直备受关注与期待。而今年,APG-2575将在ASH年会上口头报告的其首次联合acalabrutinib/利妥昔单抗治疗R/R CLL/SLL患者的数据呈现了良好的安全性和疗效,进一步表明该品种在联合治疗领域具有巨大潜力和临床价值,这令我们无比振奋。
未来,我们将进一步加快公司在研品种在全球层面的临床开发。早日造福中国乃至全球的患者。”
亚盛医药入选2022 ASH年会口头报告的研究摘要如下:
Olverembatinib (HQP1351) Overcomes Ponatinib Resistance in Patients with Heavily Pretreated/Refractory Chronic Myeloid Leukemia (CML) and Philadelphia Chromosome-Positive Acute Lymphoblastic Leukemia (Ph+ ALL)
奥雷巴替尼(HQP1351)可克服既往接受过深度治疗/难治性慢性髓细胞白血病(CML)和费城染色体阳性急性淋巴细胞白血病(Ph+ ALL)患者对于Ponatinib的耐药
展示形式:口头报告
摘要编号:162387
分会场:632.慢性髓细胞白血病:临床及流行病学进展:新型药物
Session: 632. Chronic Myeloid Leukemia: Clinical and Epidemiological: Novel Agents
l报告时间:美国东部时间2022年12月10日,星期六,上午10:15 /北京时间2022年12月10日,星期六,晚上11:15
Time: Saturday, December 10, 2022, 10:15 AM (Eastern Time) / Saturday, December 10, 2022, 11:15 PM (Beijing Time)
核心要点:
奥雷巴替尼是一种新型的第三代BCR-ABL1 TKI,对 CML 和 Ph+ ALL 具有抗肿瘤活性,且耐受性良好。
这项多中心、开放标签、随机对照的临床研究首次报告了奥雷巴替尼在中国以外的CML和Ph+ ALL患者中的安全性、有效性和药代动力学(PK)特征。这些患者至少对2种BCR-ABL1抑制剂耐药或不耐受,其中包括ponatinib和asciminib;但携带T315I突变的患者既往治疗线数不受限制。患者以3:3:2的比例随机分配到奥雷巴替尼30、40或50mg 的试验组中,采用隔日给药(QOD)的方式,28天为一个治疗周期。
共有30例患者入组,其中包括CML-CP患者 23例,CML-AP患者4例,CML急变期(-BP)患者2例,Ph+ ALL 患者1例。他们的中位(范围)治疗持续时间为4.8(0.03-21.29)个月,从诊断为CML或Ph+ ALL到开始使用奥雷巴替尼治疗的中位(范围)时间为7.0(1.5-24.0)年。半数(15/30)患者为男性,中位(范围)年龄为47.0(21.0-74.0)岁。在这些患者中,分别有1(3.3%)、7(23.3%)、8(26.7%)和9(30.0%)例患者曾经接受过2、3、4和≥5种TKI治疗;共有21例(70.0%)的患者曾经接受过第三代TKI ponatinib治疗,其中耐药17例(81.0%),不耐受4例(19.0%);共有5例(16.7%)患者曾经使用过asciminib;共有12例(40.0%)患者伴有T315I 突变;共有13例患者(43.3%)有高血压。
安全性:奥雷巴替尼的耐受性良好,22例(73.3%)患者经历了任何级别的治疗相关不良反应(TRAE),其发生率呈剂量依赖性。大多数非血液学TRAE为 1/2级;常见的3/4级血液学TRAE包括血小板减少症(7/30;23.3%)、中性粒细胞减少(5/30;16.7%)和白血球减少症(4/30;13.3%)。在所有30例患者中,有11例(36.7%)出现了严重不良反应(SAE),其中6例(20.0%)被认为与奥雷巴替尼相关并有1例(3.3%)中断治疗。来自50 mg剂量组的一例CML-AP患者死于疾病进展(PD)。
初步疗效:奥雷巴替尼在CML和Ph+ ALL患者中具有强效的抗白血病活性。在21例疗效可评估的患者中,10/17例(58.8%)获得完全细胞遗传学反应(CCyR);9/21(42.9%)的患者获得主要分子反应(MMR)。奥雷巴替尼对T315I突变的患者(62.5%,CCyR;50%, MMR)和不伴有T315I突变的患者(55.6%,CCyR;38.5%,MMR)都有效,其有效性并未因先前使用过ponatinib或asciminib而受到影响。对ponatinib耐药的患者中有5/9例(55.6%)获得CCyR,6/11例(54.5%)获得了MMR。使用过asciminib的5例患者中有4 例获得缓解。PK分析表明,奥雷巴替尼的血浆暴露量从30到50mg QOD呈剂量比例增加,中国和美国CML患者群体的血浆暴露量相当。
结论:奥雷巴替尼在难治性CML和Ph+ ALL患者中具有良好的有效性和耐受性。即使在ponatinib或asciminib耐药或有T315I 突变的患者中,其也显示出很强的疗效。该研究证实,奥雷巴替尼是CML和Ph+ ALL患者的一种潜在治疗选择,包括那些ponatinib治疗失败或T315I突变的患者。
Updated Results of Pivotal Phase 2 Trials of Olverembatinib (HQP1351) in Patients (Pts) with Tyrosine Kinase Inhibitor (TKI)-Resistant Chronic- and Accelerated-Phase Chronic Myeloid Leukemia (CML-CP and CML-AP) with T315I Mutation
奥雷巴替尼(HQP1351)治疗酪氨酸激酶抑制剂(TKI)耐药的T315I突变慢性髓细胞白血病慢性期和加速期(CML-CP和CML-AP)患者的关键性II期临床试验最新结果
展示形式:口头展示
摘要编号:170698
分会场:632. 慢性髓细胞白血病:临床及流行病学进展:新型药物
Session: 632. Chronic Myeloid Leukemia: Clinical and Epidemiological: Novel Agents
报告时间:美国东部时间2022年12月10日,星期六,上午10:30/北京时间2022年12月10日,星期六,晚上11:30
Time: Saturday, December 10, 2022, 10:30 AM (Eastern Time) / Saturday, December 10, 2022, 11:30 PM (Beijing Time)
核心要点:
T315I突变可产生高度的耐药性,对第一代和第二代TKIs都具有高度耐药性。奥雷巴替尼是一种新型的具有口服活性的第三代BCR-ABL1 抑制剂,在I期试验结果良好的基础上,开展了HQP1351-CC-201和HQP1351-CC-202两个关键性临床试验,研究数据显示在伴随T315I突变的CML-CP以及CML-AP的患者治疗中,奥雷巴替尼表现出很强的疗效以及良好的耐受性。
HQP1351-CC-201研究(CML-CP)
截止到2022年4月30日,共有41名患者入组,其中21名(51.2%)为男性,中位(范围)年龄为47(22-70)岁,从诊断为CML到首次服用奥雷巴替尼的中位时间为5.31(0.6-23.2)年,32名(78.1%)患者既往接受过≥2种TKIs。中位(范围)治疗时间为32.7(3.1-36.7)个月。
初步疗效:100%的CML-CP患者获得完全血液学反应(CHR)(31/31,其他10名患者在基线时即为CHR),34/41(82.9%)获得主要细胞遗传学反应(MCyR),29/41 (70.7%)获得 CCyR,24/41 (58.5%)获得MMR。获得CHR的中位时间为1个月(95% CI:1.0-1.9),获得MCyR的中位时间为2.8个月(95% CI:2.8-5.6),获得MMR的中位时间为6.5个月(95% CI:2.8至未达到[NR])。36个月时的无进展生存率(PFS)为86.3%(95% CI:70.2%-94.1%),总生存率(OS)为95.1%(95% CI:81.9%-98.8%)。共有5名患者因PD退出,4名患者因不耐受退出,3名患者同意退出,2名患者因其他原因退出。
安全性:常见的TRAE(所有级别;3-4级;SAEs)依次为血小板减少症(70.7%;48.8%;7.3%)、贫血(70.7%;31.7%;2.4%)、白血球减少症(51.2%;14.6%;0)、中性粒细胞减少症(41.4%;21.9%;0)。常见非血液学TRAE(所有分级; 3-4级)包括皮肤色素沉着(56.1%;0%)和肌酸激酶升高(56.1%;19.5%)、谷丙转氨酶(ALT)升高(43.9%;2.4%)和谷草转氨酶(AST)升高(36.6%;0)。
HQP1351-CC-202研究(CML-AP)
截止到2022年4月30日,共有23名患者入组,其中18名(78.3%)为男性,中位(范围)年龄为41(21-74)岁,患者从诊断为CML到首次使用奥雷巴替尼治疗的时间为4.96(0.4-10.2)年,19名(82.6%)患者既往接受≥2种TKIs。中位(范围)治疗时间为19.7 (1.4-36.4)个月。
初步疗效:共有18(78.3%)例患者获得主要血液学反应(MaHR)(73.9% CHR和4.4%无白血病证据[NEL]);12(52.2%)例患者获得MCyR;12(52.2%)例患者获得CCyR;11(47.8%)例患者获得MMR。获得MaHR的中位时间为2.8个月(95% CI:1.0-4.7);获得MCyR的中位时间为5.6个月(95% CI:2.00-NR);获得MMR的中位时间为13.1个月(95% CI:5.6-22.4)。36个月时,PFS率为57.1%(95% CI:33.3%-75.1%),OS率为69.6%(95% CI:46.6%-84.2%)。6例患者因PD退出,4例患者不耐受, 1例患者有其他原因,2例患者死亡。
安全性:常见的TRAE(所有级别;G3-4;SAEs)包括血小板减少症(78.3%;56.5%;17.4%)、贫血(69.6%;34.8%;13.0%)、白血球减少症(56.5%;30.4%;0)、中性粒细胞减少症(26.1%;26.1%;0);常见的非血液学不良事件包括皮肤色素沉着(69.6%)、低钙血症(52.2%)、蛋白尿(56.5%)、高甘油三酯血症(60.9%)、高磷血症(47.8%)、高尿酸血症(26.1%)和关节痛(34.8%),其中以1-2级居多。
结论:奥雷巴替尼对TKI耐药且伴有T315I突变的CML-CP和CML-AP患者具有良好的有效性和耐受性。基于这些关键性临床试验的结果,中国国家药品监督管理局(NMPA)药品审评中心(CDE)已于2021年11月附条件批准奥雷巴替尼上市。
A Five-Year Follow-up on Safety and Efficacy of Olverembatinib (HQP1351), a Novel Third-Generation BCR-ABL Tyrosine Kinase Inhibitor (TKI), in Patients with TKI-Resistant Chronic Myeloid Leukemia (CML) in China
新型第三代BCR-ABL酪氨酸激酶抑制剂(TKI) 奥雷巴替尼(HQP1351)在中国TKI耐药慢性髓细胞白血病(CML)患者中的5年安全性和有效性随访数据
展示形式:口头报告
摘要编号:170868
分会场:632. 慢性髓细胞白血病:临床及流行病学进展:新型药物
Session: 632. Chronic Myeloid Leukemia: Clinical and Epidemiological: Novel Agents
时间:美国东部时间2022年12月10日,星期六,上午10:00/北京时间2022年12月10日,星期六,晚上11:00
Time: Saturday, December 10, 2022, 10:00 AM (Eastern Time) / Saturday, December 10, 2022, 11:00 PM (Beijing Time)
核心要点:
这项在中国进行的开放性、多中心的I期临床试验评估了奥雷巴替尼在成年CML-CP或CML-AP患者中的安全性和有效性5年长期随访数据。符合条件的患者包括对第一代或第二代TKIs耐药或不耐受的CML-CP或CML-AP患者。奥雷巴替尼的使用方式为口服、QOD、28天为一个周期,共有范围从1至60mg的11个剂量组。
从2016年10月26日至2022年4月30日(数据截止日期),101例CML-CP(n=86)和CML-AP(n=15)患者入组并接受了奥雷巴替尼治疗。中位治疗时间为44.7(1.2-63.1)个月。71例(70.3%)患者为男性,中位年龄为40岁(范围20-64岁),从诊断到首次接受奥雷巴替尼治疗的中位(范围)时间为6.0年(0.3-15.2年)。84例(83.2%)患者接受了≥2种TKI治疗,63例(62.4%)患者携带T315I突变。在基线时,12例(11.9%)患者检测到复合突变,其中8例(66.7%)携带BCR-ABL1T315I突变。共有20例(19.9%)患者有2(n=13)或≥3(n=7)种突变。截至数据截止日期,101例患者中72例(71.3%)继续治疗,28例(21例CML-CP和7例CML-AP)因疾病进展、不耐受或其他原因停止治疗。累积药物暴露的中位剂量数(范围)为20,175(660-34,395)mg。101例患者中,79例(78.2%)治疗>3年,21例(20.8%)治疗>4年,3例(3.0%)治疗>5年。
初步疗效:在可评估的CML-CP患者中,100%的患者获得了CHR,80%获得了MCyR,71.3%获得CCyR,55.3%获得MMR;在可评估的CML-AP患者中,CHR占85.7%,MCyR、CCyR和MMR各占40%。在可评估的T315I突变患者中,CMP-CP患者的CHR为100%,MCyR为83.7%,MMR为73.1%;CML-AP患者的CHR为80.0%,MCyR和MMR各为54.5%。CML-CP患者48个月的PFS率为85.6%(95% CI:70.6%-93.3%);CML-AP患者48个月的PFS率为50.0%(95% CI:22.9%-72.2%); 奥雷巴替尼在复合突变的CML患者中表现出显著的疗效。12例经新一代基因测序技术确认携带复合突变的患者中,7例(58.0%)达到MMR;3(25.0%)例达到MR4.5。截止到最后一次随访时,3例患者进展到CML-AP或CML-BP并死亡,7例仍在接受奥雷巴替尼治疗,其中1例获得MMR,CHR、CCyR和MR4.5各2例。
安全性:大多数TRAE为1级或2级。最常见的非血液学不良事件为(多为1级或2级)皮肤色素沉着(85.1%);≥3级非血液学AEs包括高甘油三酯血症(10.9%)、发热(6.9%)和蛋白尿(6.9%)。最常见的血液学相关不良事件为血小板减少症,在79例(78.2%)患者中发生,其中52例(51.5%)≥3级和7例(6.9%)SAE;21例(20.8%)白血球减少症≥3级,无SAE;17例(16.8%)贫血≥3级,4例(4.0%)SAE。
结论:这项首次在人体实验的5年随访结果显示,奥雷巴替尼在前期接受过重度治疗的CML患者中具有持久疗效和良好的耐受性。
Lisaftoclax (APG-2575) Safety and Activity As Monotherapy or Combined with Acalabrutinib or Rituximab in Patients (pts) with Treatment-Naïve, Relapsed or Refractory Chronic Lymphocytic Leukemia/Small Lymphocytic Lymphoma (R/R CLL/SLL): Initial Data from a Phase 2 Global Study
Lisaftoclax(APG-2575)单药或与Acalabrutinib/利妥昔单抗联合治疗在初治、复发或难治的慢性淋巴细胞白血病/小淋巴细胞淋巴瘤(R/R CLL/SLL)患者中的安全性和抗肿瘤活性:来自一项II期全球性临床研究的初步数据
展示形式:口头报告
摘要编号:160386
分会场:642.慢性淋巴细胞白血病:临床及流行病学:在研药物和新冠病毒感染
报告时间:美国东部时间2022年12月12日,星期一,下午5:15/北京时间2022年12月13日,星期二,早上6:15
核心要点:
APG-2575是一种特异性Bcl-2抑制剂,在R/R CLL/SLL患者中具有活性,包括经BTKi治疗后疾病进展(PD)且伴有del(17p)的患者。这是APG-2575联合acalabrutinib或利妥昔单抗用于R/R CLL/SLL患者的数据首次报告。
患者每天单独口服APG-2575(400mg,600mg和800mg)或与acalabrutinib/利妥昔单抗联用6个周期,每28天为一周期。主要目的为确定II期研究推荐剂量(RP2D)、安全性和有效性,包括APG-2575单药及联合acalabrutinib或利妥昔单抗的ORR。在监测肿瘤溶解综合征(TLS)前提下,患者采用每天梯度递增给药的方式,4-6天后可达到最终目标剂量:第1天(D1)20mg,D2 50mg,D3 100mg,D4 200mg,D5 400mg。随后第1周期第1天(C1D1)APG-2575 的目标剂量为400、600或800mg。联合治疗组中的患者在完成梯度递增给药达到目标剂量后,继续接受额外7天的APG-2575先导治疗,然后在C1D8时加入acalabrutinib/利妥昔单抗,直至PD或者观察到不可耐受的毒性。
截止2022年7月4日,共入组141例患者。中位年龄62岁(18-80)。98例(70%)为男性,125例(89%)患者的东部肿瘤协作组(ECOG)评分为0-1分,15例(11%)为2分。既往中位治疗线数为2线(1-15)。17例(12%)患者既往使用过BTKi(n=15)和/或venetoclax(n=3)治疗出现PD。联合组中(n=95),其中TP53突变或伴del(17p)有39例(41%),del(11q)有27例(28%),IGHV未突变有36例(38%),IGHV突变有14例(15%),47%未知。中位使用APG-2575 10(0-30)个周期,包括单药组16.5个周期,利妥昔单抗联合组9(1-15)个周期,acalabrutinib联合组7(0-18)个周期。3例(2%)基线存在巨大肿块的患者报告TLS(2例临床,1例实验室),2例临床TLS的患者最终均完全恢复。联合组中,C1D8加入acalabrutinib/利妥昔单抗后,未观察到任何TLS发生。
安全性:常见的(>5%)任何级别的不良反应(AE)包括:粒细胞减少(30%,3/4级为26%),新冠病毒感染(26%),贫血(24%,3/4级为12%),腹泻(20%),血小板减少(17%,3/4级为5%),高尿酸血症或发热(各9%),恶心、头痛或疲劳(各占8%),谷草转氨酶(AST)水平升高(7%),高磷血症(6%);肌酐升高(6%)。首次3级及以上的血细胞减少发生在梯度递增或C1期间,罕见于C2(n=3 [2%])之后。13%患者在生长因子支持下≥3级的中性粒细胞减少的不良事件可控。未观察到剂量限制毒性(DLT)。联合治疗组中未发现药物相互作用。
初步疗效:56%的患者在每天梯度递增给药结束后,淋巴细胞迅速恢复至正常水平。单药组中,患者的ORR达65%(43例);acalabrutinib联合组中,患者的ORR达98%(53例),利妥昔单抗联合组中,患者的ORR达87%(23例)。
结论:在初治及R/RCLL/SLL患者中,每日梯度剂量递增给药的情况下,APG-2575单药或与acalabrutinib/利妥昔单抗联合治疗的安全性可控,并展示出了优异的早期疗效。




 扫码下载智通APP
扫码下载智通APP