礼来(LLY.US)阿尔茨海默病新药在中国获批临床
智通财经APP获悉,1月16日,中国国家药监局药品审评中心(CDE)官网公示,礼来公司(LLY.US)(Eli Lilly and Company)的1类新药remternetug注射液获得临床试验默示许可,拟开发治疗早期阿尔茨海默病。公开资料显示,remternetug靶向一种名为N3pG的淀粉样蛋白亚型,目前正在海外进行一项治疗早期阿尔茨海默病患者的3期临床试验。值得一提的是,近日,礼来另一款靶向N3pG的β淀粉样蛋白斑块的阿尔茨海默病疗法donanemab注射液还被CDE纳入突破性治疗品种。
据悉,此次remternetug在中国获批临床,意味着该产品也将在中国进入临床研究阶段。

截图来源:CDE官网
阿尔茨海默病是一种主要与衰老相关的神经退行性疾病,疾病进展包含在思考、记忆与行为上的改变,疾病最终会在几年内进展成痴呆症。阿尔茨海默病并非正常的老化过程,在患者症状开始前20年,其脑部便出现复杂的变化,最终造成脑细胞死亡或联结丧失。
研究发现,阿尔茨海默病以突触丧失和神经元死亡引起的认知障碍为特征,细胞外β淀粉样斑块是其病理标志之一。靶向淀粉样蛋白是阿尔茨海默病新药开发的重要方向之一。近日(1月7日),美国FDA还批准了第二款靶向β淀粉样蛋白的创新阿尔茨海默病疗法。
根据礼来公司公开资料,remternetug(LY3372993)是一款下一代N3pG淀粉样蛋白抗体,采用灵活的给药方案,包括皮下给药,以满足阿尔茨海默病患者的不同需求。此前,该产品已在1b期临床试验中显示出与淀粉样蛋白降低等级一致的深度斑块清除,并且具有较好的安全性。
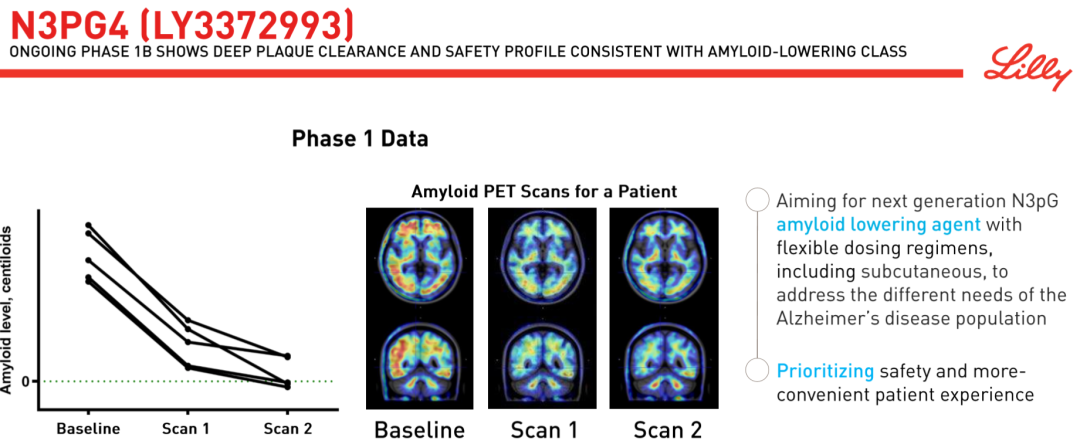
截图来源:礼来2021年研发日PPT
根据ClinicalTrials网站,目前remternetug正在开展两项临床试验,其中一项是名为TRAILRUNNER-ALZ 1的随机、双盲、安慰剂对照、3期研究,旨在评估候选药对早期症状性阿尔茨海默病患者的安全性和有效性。该试验计划在美国和日本共计入组400人,受试者将通过皮下注射或静脉输注接受remternetug或安慰剂治疗。




 扫码下载智通APP
扫码下载智通APP