新股解读|“破发”噩梦之下,信达生物说他比“O”“K”药还牛
顶着新股市场的巨大压力,港股第四家未盈利生物科技企业——信达生物,终于迎来了自己的表演时间。
从已上市的三家企业来看,未盈利生物科技企业确实不受市场“待见”,特别是顶着“未盈利生物科技企业第一股”头衔的歌礼生物—B(01672)格外“凄惨”,截至10月8日收盘,较发行价跌超50%。
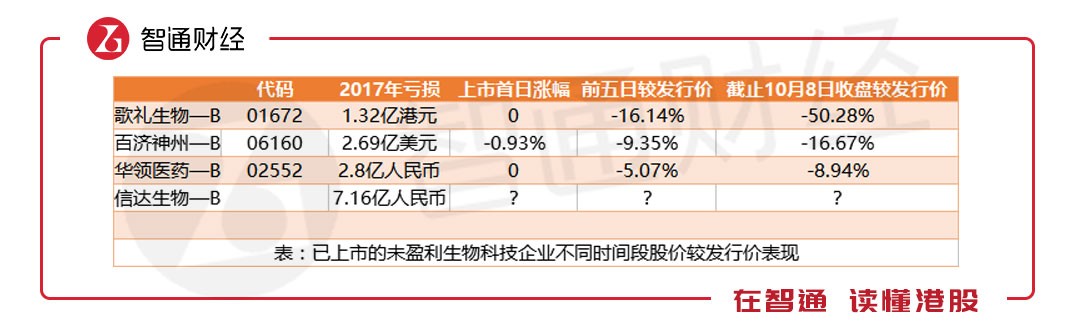
不过能明显看到的是,在歌礼生物—B“以身试法”之后,百济神州—B(06160)、华领医药—B(02552)的表现无疑要好很多。那么,在市场对未盈利生物科技企业逐渐熟悉之后,信达生物能否逃离破发“魔咒”?
17条研发管线
信达生物是本土创新药物研发的代表企业,该公司在成立至今的七年时间中,开发了全面集成的生物医药平台,将研究、发现、开发、制造和商业化能力整合为一体。
依靠该生物医药平台,信达生物建立了一个由17种抗体候选药物组成的产品研发管线。其中,拥有全球化专利的四种核心产品已在中国进入后期临床开发阶段,包括新型的PD-1抗体信迪利单抗IBI-308,以及三种生物类似药IBI-301、IBI-303、IBI-305。
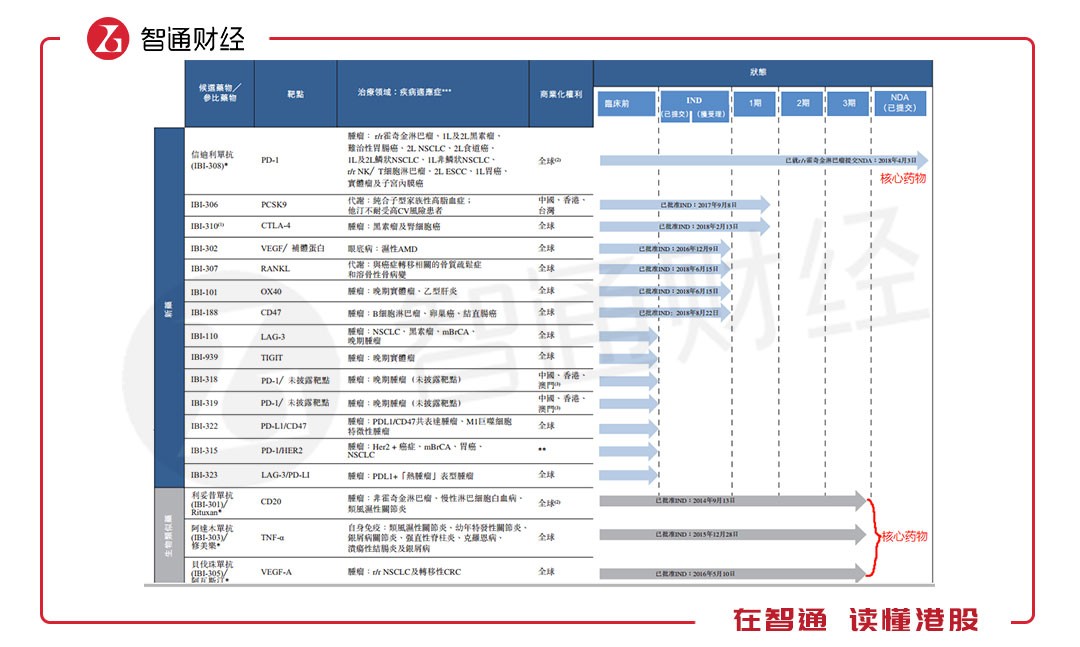
信迪利单抗IBI-308是基于PD-1靶点的肿瘤治疗药物,信达生物已于2018年4月3日就用于治疗r/r霍奇金淋巴瘤的信迪利单抗提交了新药上市申请,4月16日已获国家药品监督管理局受理,并于4月23日被纳入优先评选程序。
倘若获国家药品监督管理局批准,公司计划于2019年推出信迪利单抗。与此同时,信达生物已取得美国食用药品监督管理局有关信迪利单抗临床实验申请授出的批准,并计划在美国启动IBI-308的多中心1b/2期临床试验。
而三种生物类似药正在进行3期临床试验,分别是治疗肿瘤的IBI-301、IBI-305,以及治疗自身免疫疾病的IBI-303,三种药物预计在2019年提交新药申请。
除了四种核心药物之外,信达生物还有6种药物已通过了临床试验申请,其中的IBI-306、IBI-310已进入了临床1期。剩余的7种药物,均处于临床前的研发阶段。
单从研发管线而论,信达生物的研发药物多样,且研发进度有所分类,先后有序,保证了短中长期药物商业化的可能,有利于长期发展。
信利单抗的两大优势
据智通财经APP了解,PD-1抑制剂是近年来肿瘤免疫疗法研究的热点,其药物作用机制与手术、放化疗及靶向药等有很大不同,PD-1抑制剂并不是直接杀死癌细胞,而是通过激活病人的自身免疫系统抗癌。
PD-1抑制剂包括PD-1抗体和PD-L1抗体,截至2018年5月10日,全球共有5种已上市的PD-1及PD-L1抗体,包括PD-1抗体的Keytruda(K药)及Opdivo(O药),PD-L1抗体的Tecentriq、Bavencio及Imfinzi。
信达生物的信迪利单抗IBI-308便是PD-1抗体药物,据招股书显示,公司的该药物有望成为同类中最佳的创新性PD-1单克隆抗体。在对中国96例经典霍奇金淋巴患者进行治疗的注册临床试验中,信迪利单抗IBI-308显示出了79.2%(第24周数据)的总体缓解率(ORR)和17.7%(第15周数据)的完全缓解率(CR),其安全性及毒性特征可与现已获批准的PD-1抗体相媲美。
且信迪利单抗IBI-308在生物特性上有所改善,与O药和K药相比,具有以下的竞争优势:
其一,对PD-1具有更高的结合亲和力。体外研究表明,信迪利单抗对PD-1的结合亲和力比K药和O药的结合亲和力分别高出约10倍、50倍。
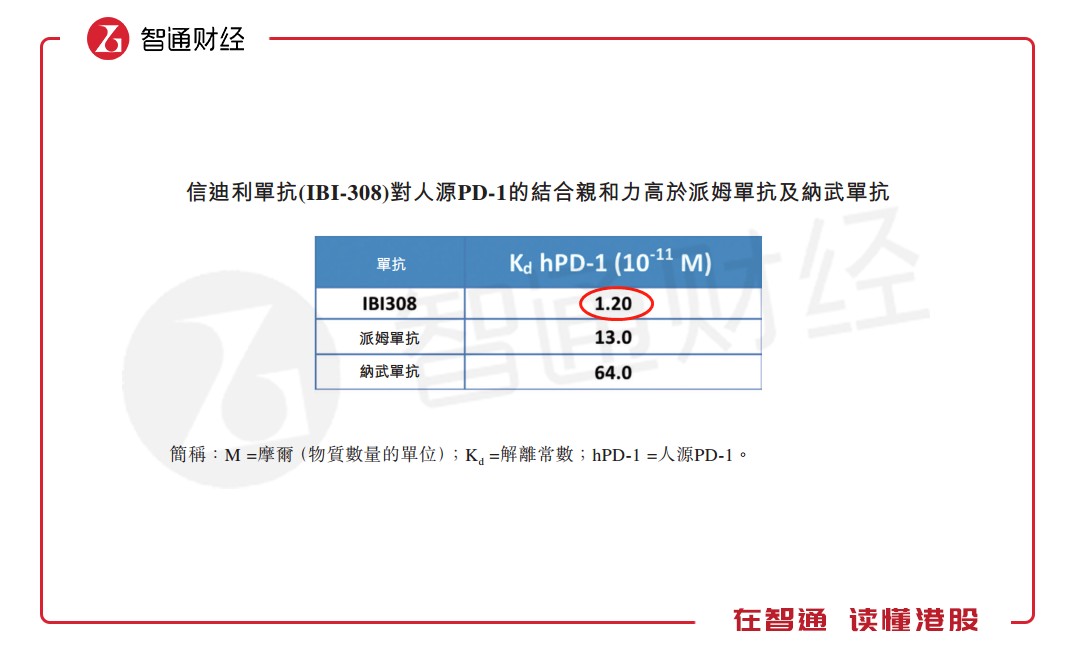
其二,信迪利单抗能结合更多的靶点占位。在3mg/kg的剂量水平下,信迪利单抗在治疗周期的整个持续时间段内具有高于95%的靶点占位,相比之下,同样剂量的O药在整个治疗周期中仅具有75%-80%范围内的靶点占位。
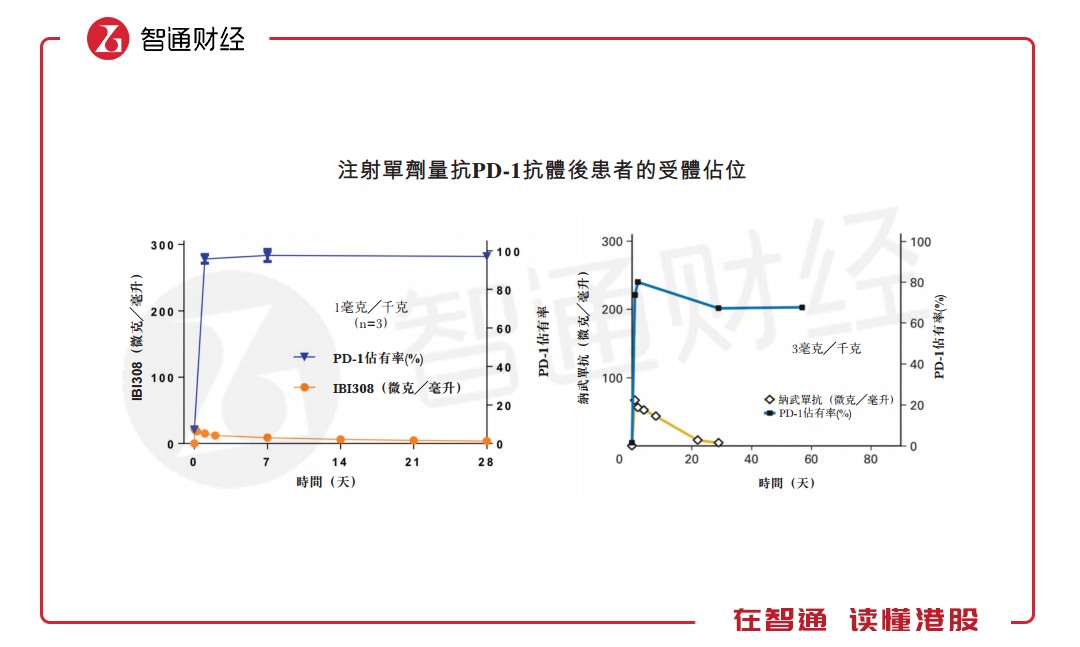
基于以上两点,信利单抗在相同剂量水平及相同给药频率下将取得比目前市场上已有同类药物更好的治疗效果,这对于身受癌症折磨的患者而言,与“神药”无异。
市场规模增速534.4%
在有好产品的同时,信达生物所面对的是庞大的市场。据数据显示,中国所有癌症的发病率由2013年的370万人增至2017年的420万人,年复合增长率3.4%。由于不健康的生活方式及污染加剧等因素,中国所有癌症的发病率预计于2017年至2022年间按2.6%的年复合增长率增至2022年的480万人。
在国内几百万患者的需求下,中国PD-1及PD-L1抗体药物将迎来爆发式的增长。据弗若斯特沙利文报告显示,中国PD-1及PD-L1抗体的市场规模将从2018年的0收入增至2022年的374亿人民币,年复合增长率高达534.4%。从2022至2030年,该市场仍将保持超过10%的增长速度。
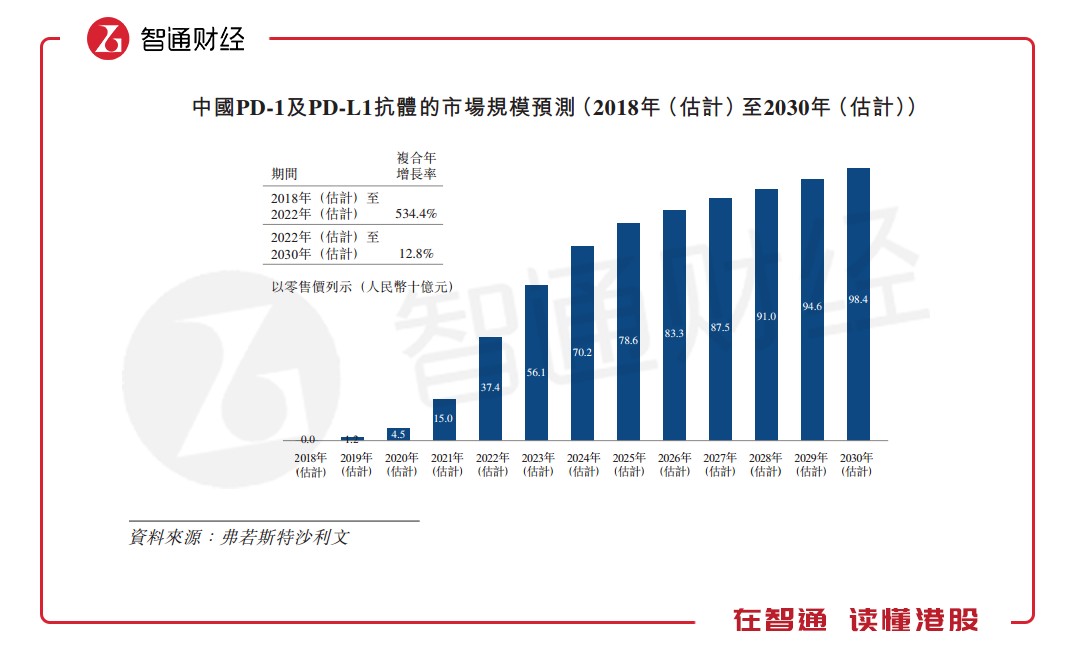
与此同时,随着生物类似药监管途径的设立以及大量知名生物药物的专利到期,中国生物类似药市场也将蓬勃发展。弗若斯特沙利文预计,从2017年到2022年,中国生物类似药将按70.9%的年复合增长率增长,从2022年至2030年,有望按16.8%的年复合增长率继续增长。
且信达生物目前所研发的17种管线产品中,有13种已确定拥有全球商业化潜力,在“享受”国内暴增市场的同时,可向海外开拓更大市场。
同类药物齐出,商业化竞争加剧
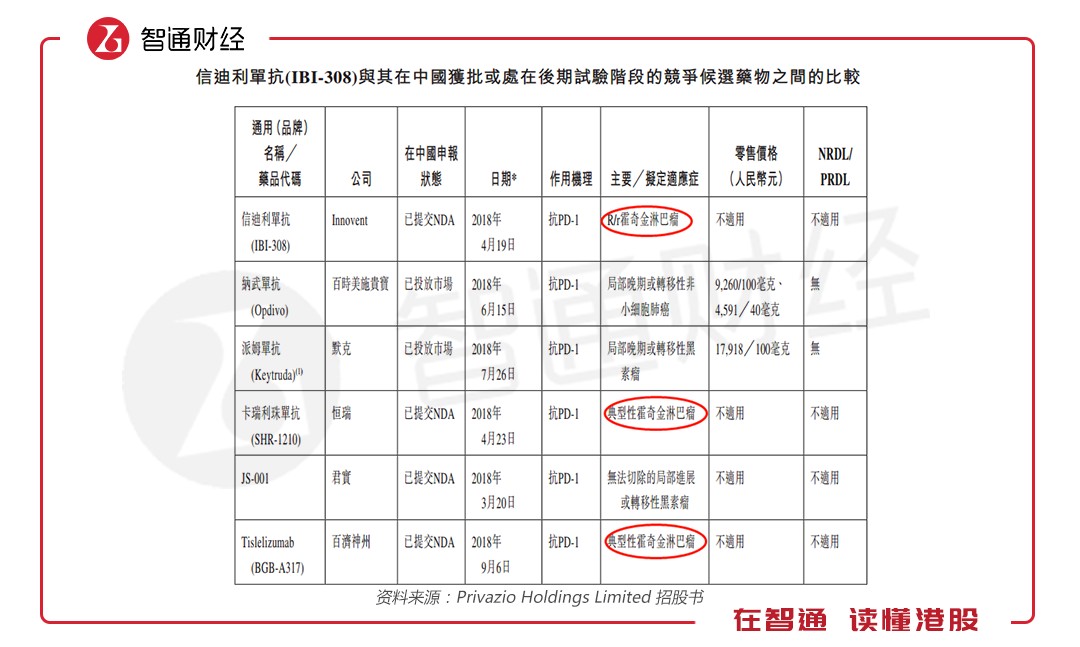
前景看似一片大好,但信达生物面临着商业化竞争加剧的压力。截至目前,与信迪利单抗作用机理相同,处于竞争状态的药物有5种,这其中包括“外来药”O药及K药,该两种药物均已获得国家药物监督管理局的批准可投入中国市场;且价格较美国零售价有较大折价,增大了“外来药”的竞争优势。截止目前,O药在中国的售价为美国零售价的52.9%,K药在中国的售价为美国零售价的54%。
信迪利单抗不仅要与“外来药”竞争,还得与“国产药”一争高下。与信迪利单抗一样,恒瑞的SHR-1210、君实的JS-001、百济神州的BGB-A317均已提交新药申请,预计可在2019年推向市场,且恒瑞的SHR-1210、百济神州的BGB-A317这两个药物的主要适应症都是霍奇金森淋巴瘤,与信迪利单抗适应症极为相似。
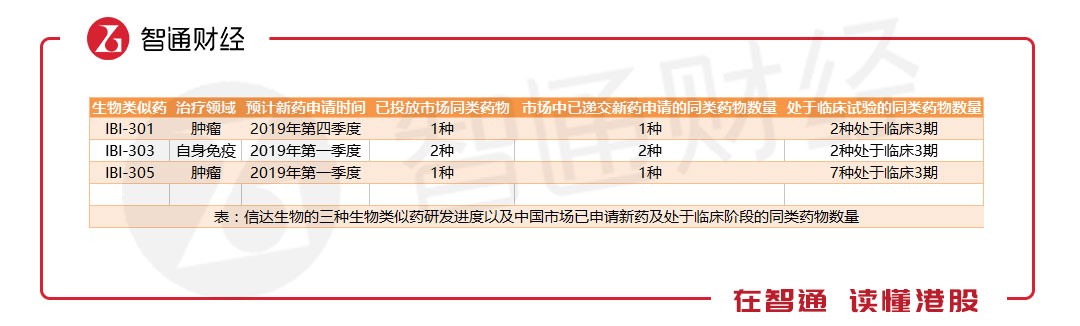
与此同时,信达生物剩余三种核心生物类似药也面临竞争难题。目前,市场中与IBI-301同类的药物已有1种投入市场,1种递交新药申请,2种处于临床3期;IBI-303的同类药物已有2种投入市场,2种递交新药申请,2种处于临床3期;IBI-305的同类药物已有1种投入市场,1种递交新药申请,7种处于临床3期。
总的来看,国内市场正处于爆炸式增长阶段,信达生物产品线丰富,信迪利单抗药性优于O药及K药,但在各方角逐的情况下,“刀光剑影”自然少不了。有同类药物的百济神州股价已跌超发行价15%,还是小心为妙。



 扫码下载智通APP
扫码下载智通APP