研发投入最多,这10家药企榜上有名
本文来自微信公众号“药明康德”。
2018年是新药获批创纪录的一年,而这一年,世界上15大生物医药公司投入研发的资金数目也首次跨过了1000亿美元的大关。虽然根据IQVIA最近的报告,在新药研发领域,新兴医药公司对研发创新的贡献越来越重要,但是大型医药公司在新药开发方面仍然具有不可忽视的影响。
近日,“FierceBiotech”公布了2018年药物研发投入最多的10大药企。药明康德内容团队将与读者分享这些大型药企在研发投入方面的最新进展和布局。

▲大型药企研发投入数额和占销售额比例一览(图片来源:FierceBiotech官网)
公司:罗氏(Roche)
研发投入:109.8亿美元
研发投入占销售额比重:19.3%

罗氏一直是生物医药领域研发投入最多的公司之一。该公司2018年的研发投入比2017年增长了6%。该公司有16款新分子实体(new molecular entities, NME)处于临床后期研发阶段。
其中两款新药预计在今年获批。“first-in-class”抗CD79b抗体偶联药物(ADC)polatuzumab vedotin已于昨日提前2个月获得FDA加速批准,与苯达莫司汀与rituximab联用,治疗难治的弥漫性大B细胞淋巴瘤(DLBCL)成人患者。这一组合疗法与标准疗法相比,能够将患者的完全缓解率提高一倍有余。
另一款今年可能获得批准的创新药是“不限癌种”的精准疗法entrectinib,它是一款能够在中枢神经系统(CNS)中生效的ROS1/NTRK/ALK小分子抑制剂。在上周刚结束的美国临床肿瘤学会(ASCO)年会上公布的最新数据表明,对于携带NTRK,ROS1或ALK基因融合的实体瘤儿科患者来说,entrectinib达到100%的总缓解率。
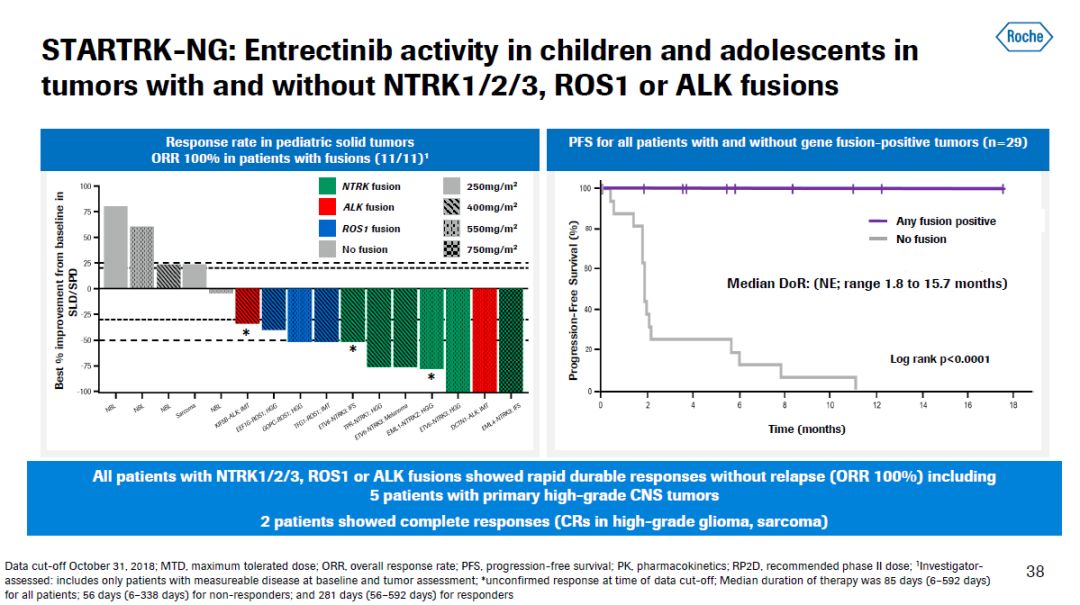
图片来源:参考资料[2]
除了这两款新药以外,治疗视神经脊髓炎的抗IL-6抗体satralizumab可能在今年递交监管申请,它已经获得了FDA授予的突破性疗法认定。治疗脊髓性肌肉萎缩症(SMA)的口服疗法risdiplam也获得了积极的临床试验结果,有望在今年递交监管申请。如果获得批准,将为SMA患者带来除了基因疗法和反义寡核苷酸疗法以外的口服治疗选择。
公司:强生(Johnson & Johnson)(JNJ.US)
研发投入:107.6亿美元
研发投入占销售额比重:13.2%

强生公司在世界各地构建的JLABS研发基地帮助将早期科学突破转化成尖端创新药物和科技。近日,强生旗下的杨森(Janssen Pharmaceutical Companies)公司表示,该公司有望在2019-2023年期间推出至少10款重磅新药!
其中,治疗尿路上皮癌的“first-in-class”特异性FGFR抑制剂Balversa(erdafutinib)和治疗成年治疗抵抗性抑郁症患者的Spravato(esketamine)已经分别在今年4月和3月获得FDA的批准。
出了上述公布的潜在重磅新药以外,强生公司还致力于开发多种创新治疗模式的技术平台,其中包括细胞疗法,RNAi疗法,和基因疗法等等。
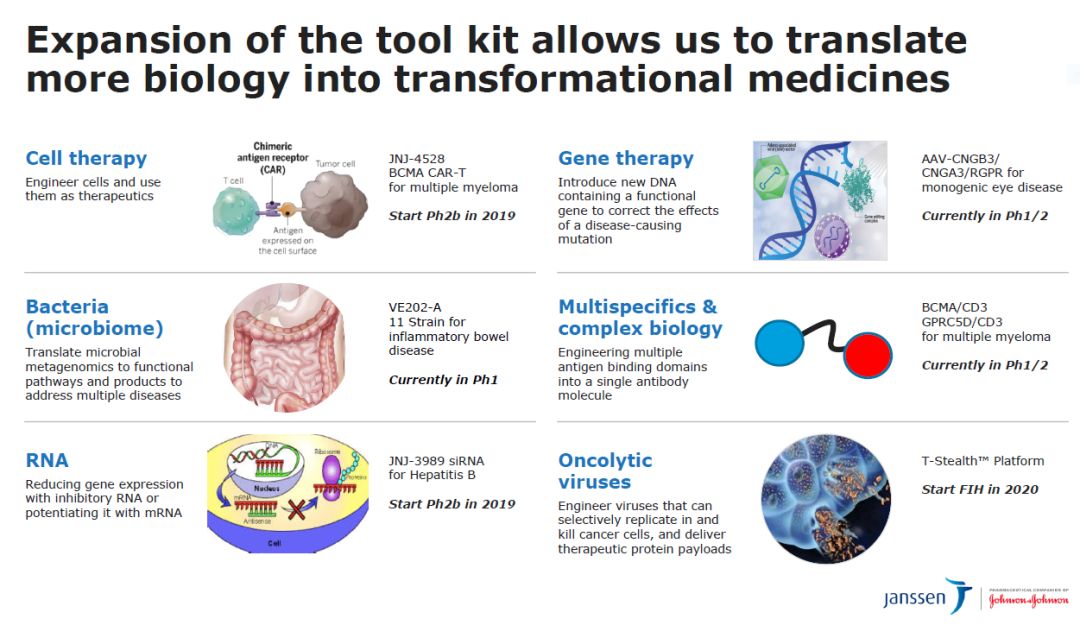
▲杨森公司的多种在研疗法技术平台(图片来源:参考资料[3])
该公司与中国的南京传奇合作开发靶向BCMA的CAR-T疗法和公司内部开发的靶向血红素的CAR-T疗法将是强生公司近期细胞疗法的主攻方向。杨森同时在提高自身制造细胞疗法的生产能力,并且开发解决自体疗法局限的下一代细胞疗法。
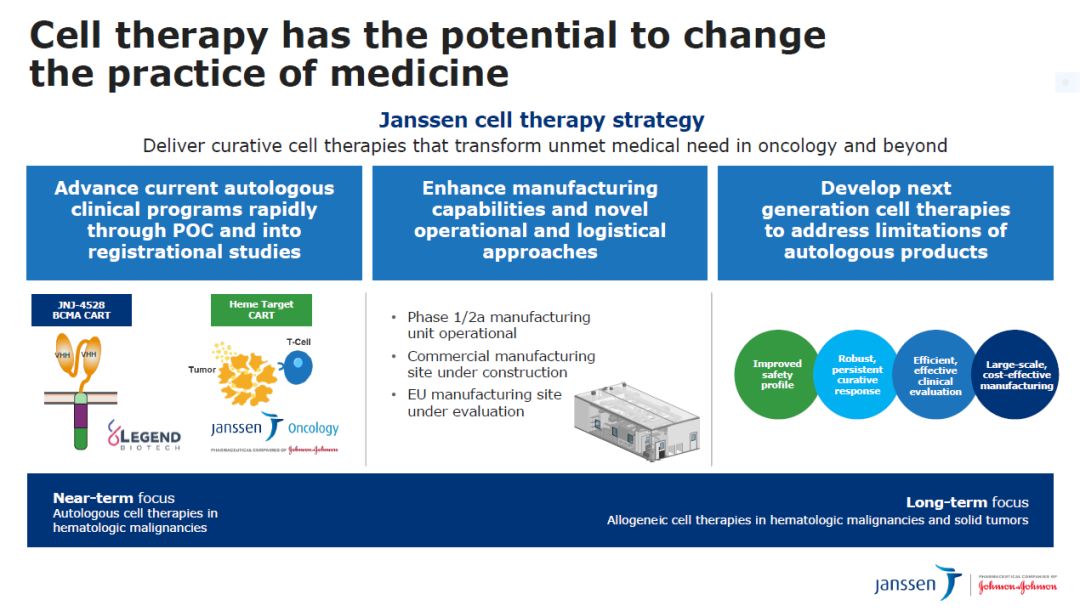
图片来源:参考资料[3]
在基因疗法方面,杨森的研发策略是首先靶向眼睛这类解剖学上隔离的器官。该公司与MeiraGTx今年达成研发合作,共同开发治疗遗传性视网膜疾病的基因疗法。
该公司还与Arrowhead公司去年达成研发合作,开发治疗乙肝的RNAi创新疗法。这是杨森公司利用基因沉默技术开发创新疗法的策略之一。
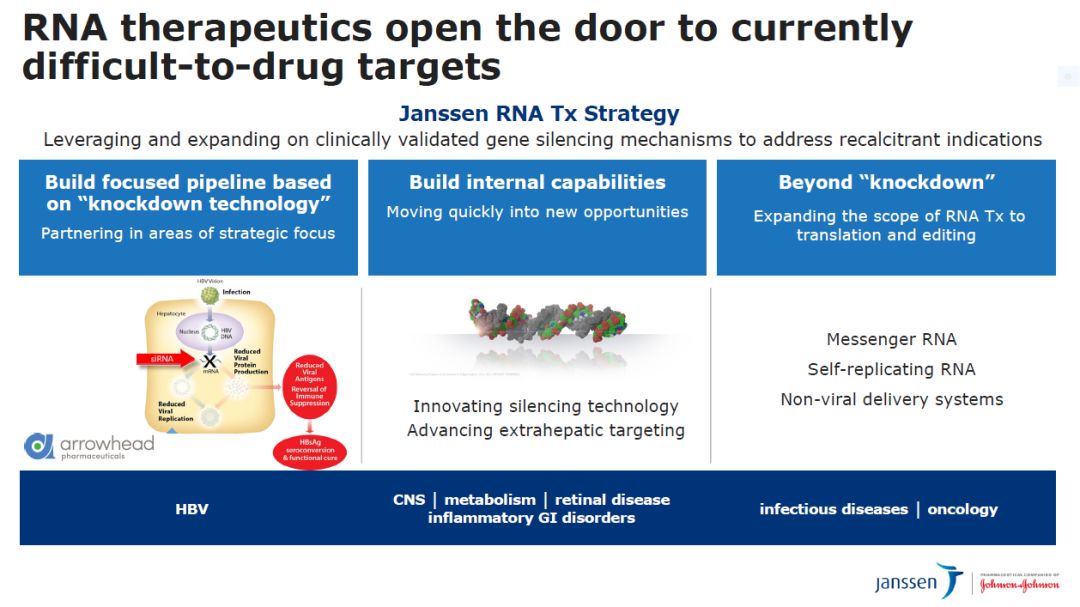
图片来源:参考资料[3]
公司:默沙东(MSD)(MRK.US)
研发投入:97.5亿美元
研发投入占销售额比重:23%

默沙东目前在进行超过1000项临床试验,检测其重磅抗癌免疫检查点抑制剂Keytruda治疗不同类型癌症的疗效。这款抗PD-1抗体的表现也非常出色,今日又获得FDA批准,成为治疗头颈癌的一线疗法。
今年Keytruda还获得批准扩展其治疗非小细胞肺癌患者的范围,与Inlyta联用一线治疗晚期肾细胞癌患者,以及作为辅助疗法,在手术切除后治疗黑色素瘤转移到淋巴结中的癌症患者。
除了Keytruda,默沙东还在疫苗领域有深入布局,目前有4款疫苗处于临床后期研发阶段。其中包括预防埃博拉病毒的疫苗和预防儿童肺炎的15价肺炎疫苗。这款疫苗已经获得FDA授予的突破性疗法认定,并且在日前达到2期临床终点。
公司:诺华(Novartis)(NVS.US)
研发投入:91亿美元
研发投入占销售额比重:17.5%

诺华公司对研发的投入一直在大型药企中名列前茅。这些投资在2019年也将带来不俗的收获。迄今为止,该公司已有三款重磅新药获批,分别是治疗多发性硬化症(MM)的Mayzent(siponimod),治疗SMA的基因疗法Zolgensma,和第一款治疗携带PIK3CA突变的PI3K抑制剂alpelisib。该公司今年预计还可能有一款潜在重磅新药获批,它是治疗湿性AMD的双特异性抗体brolucizumab。
该公司未来3年中将可能有10余款重磅新药上市,关于这些新药的信息药明康德内容团队已经在日前做过详细介绍。除此以外,根据诺华内部评估,该公司2019年的药物研发管线中73%的研发项目可能成为“first-in-class”药物。

图片来源:参考资料[4]
在基因疗法方面,通过收购AveXis公司,诺华的基因疗法技术平台目前包含了9个研发项目。该公司还通过与Lutathera的合作和收购Endocyte公司构建了放射性配体(radioligand)疗法平台,目前这一技术平台中有多项药物研发项目,用于治疗前列腺癌、乳腺癌、神经母细胞瘤等癌症。
公司:辉瑞(Pfizer)(PFE.US)
研发投入:80.1亿美元
研发投入占销售额比重:14.9%

辉瑞公司在去年进行了结构重组,将所有新药研发项目纳入一个名为辉瑞生物医药(Pfizer Biopharmaceuticals)的部门。截至2019年4月30日,该公司的研发管线中包括97个研发项目,其中30个处于2期临床阶段,23个处于3期临床阶段,10个处于监管申请阶段。其中可能有15个潜在重磅药物在2022年之前获得批准。

图片来源:参考资料[5]
这些研发项目中的一个重心是与德国默克(Merck KGaA)合作开发的PD-L1抗体Bavencio(avelumab)。目前有30个临床研究检测Bavencio作为单药或组合疗法的一员,治疗15种不同癌症类型的疗效。近日,Bavencio和Inlyta构成的组合疗法已经获得FDA批准,一线治疗晚期肾细胞癌患者。
该公司开发的tafamidis已经获得FDA批准上市,用于治疗因为野生型或遗传性转甲状腺素蛋白介导的淀粉样变性引起的心肌病(ATTR-CM)。这是FDA批准的第一款治疗ATTR-CM的疗法。
在处于后期研发阶段的研发项目中,治疗特应性皮炎的JAK1抑制剂abrocitinib在3期临床试验中获得积极顶线结果。与礼来(Eli Lilly)合作开发的NGF抑制剂tanezumab也在治疗多种慢性疼痛的3期临床试验中达到主要终点。
基因疗法正在成为大型医药公司布局的重点领域,辉瑞也在今年与Vivet Therapeutics公司达成研发合作,开发治疗治疗威尔逊病(Wilson Disease)的基因疗法,并且有权利通过收购Vivet公司,获得其所有基于创新腺相关病毒(AAV)技术的在研产品。
公司:赛诺菲(Sanofi)(SNY.US)
研发投入:66.6亿美元
研发投入占销售额比重:17.1%

前罗氏药物研究和早期开发负责人John Reed博士去年加入赛诺菲,领导其研发管线的开发。在他的领导下,赛诺菲公司的研发重心将向疫苗和专科治疗领域(specialty care)转移。
今年,该公司在这两个领域也有所斩获。治疗获得性血栓性血小板减少性紫癜(aTTP)的Cablivi(caplacizumab)获得FDA批准上市。这是一款靶向抗血管性血友病因子(vWF)的纳米抗体。而该公司开发的登革热疫苗Dengvaxia也在5月份获得FDA批准。这是第一款获得FDA批准的登革热疫苗。
除此之外,该公司和Lexicon Pharmaceuticals公司联合开发的SGLT1/2双重抑制剂Zynquista(sotagliflozin)获得欧盟批准治疗1型糖尿病患者。这是这一疗法首度获批治疗1型糖尿病患者。

▲赛诺菲药物研发管线中的新分子实体(图片来源:参考资料[6])
在该公司处于临床后期研发阶段的在研疗法中,治疗复发/难治性多发性骨髓瘤(MM)的抗CD38单克隆抗体isatuximab在3期临床试验中已经获得积极结果,预计在今年递交监管申请。
在今年ASCO年会上公布的3期临床试验结果表明,将istauximab加入到pomalidomide和dexamethasone构成的组合疗法中,可以将患者的无进展生存期提高5个月(11.5个月比6.47个月),将这些患者疾病进展或死亡风险降低了40%。
公司:百时美施贵宝(BMS)(BMY.US)
研发投入:63.4亿美元
研发投入占销售额比重:28%

BMS的研发管线中,免疫检查点抑制剂一直占据着重要的位置。该公司开发的抗CTLA-4抗体Yervoy和抗PD-1抗体Opdivo是免疫检查点抑制剂中的代表性药物。BMS的很多研发投入与开展不同临床试验,检验基于免疫检查点抑制剂的组合疗法在治疗不同癌症类型中的疗效相关。BMS去年还与Nektar公司达成研发协议,开发创新免疫组合疗法。
今年年初,BMS以740亿美元收购新基(Celgene)公司,这一收购在今年四月获得股东批准,预计在今年第三季度完成。这一交易将给BMS带来丰富的研发管线,其中治疗贫血的luspatercept,治疗骨髓纤维化的JAK2抑制剂fedritinib,和治疗多发性硬化症的ozanimod都已经递交上市申请。Luspatercept和fedritinib还获得了优先审评资格,有望今年获得批准。
公司:阿斯利康(AstraZeneca)(AZN.US)
研发投入:59.3亿美元
研发投入占销售额比重:27%

阿斯利康去年对公司的结构也进行了重组,将MedImmune并入公司内部,并且将新药研发部门分为肿瘤学和生物医药(包括非肿瘤学的研发项目)两大块。

图片来源:参考资料[6]
肿瘤学是阿斯利康公司的研发重心,该公司拥有多样化的抗癌产品组合和研发项目。在刚刚结束的ASCO年会上,该公司与默沙东联合开发的PARP抑制剂Lynparza在治疗胰腺癌的3期临床试验中,显著延长携带生殖系BRCA突变(gBRCAm)患者的无进展生存期。
该公司斥资69亿美元与第一三共(Daiichi Sankyo)联合开发的靶向HER2的抗体偶联药物trastuzumab deruxtecan在治疗多种HER2+癌症中也表现出卓越的疗效,有望在今年递交监管申请。

图片来源:参考资料[7]
预计在2019年下半年,阿斯利康公司将递交近10项监管申请,其中包括在中国获得首批的治疗肾性贫血的roxadustat。
公司:礼来(Eli Lilly)(LLY.US)
研发投入:53.1亿美元
研发投入占销售额比重:23.2%

礼来公司在今年年初宣布以80亿美元的价格收购开发精准疗法的Loxo Oncology公司,并且获得了该公司的三款靶向抗癌疗法,包括一款新一代TRK抑制剂,一款口服BTK抑制剂,和名为LOXO-292的RET抑制剂。LOXO-292已经获得了FDA授予的突破性疗法认定,用于治疗RET+甲状腺癌和非小细胞肺癌患者。
礼来的药物研发管线中,血管内皮生长因子2(VEGFR2)拮抗剂Cyramza(ramucirumab)获得FDA批准,治疗甲胎蛋白(AFP)水平高于400 ng/ml,接受过sorafenib治疗的肝细胞癌患者。CGRP抗体Emgality(galcanezumab-gnlm)也在上周获得FDA批准治疗阵发性丛集性头痛成人患者。
礼来公司有多款靶向IL-23/IL-17这一明星信号通路的获批和在研疗法。其中,靶向IL-17A的Taltz(ixekizumab)在治疗治疗非放射性轴性脊柱关节炎(nr-axSpA)的3期临床试验中,达到主要终点和所有重要的次要终点。它可能成为第一款治疗nr-axSpA的IL-17A拮抗剂。而靶向IL-23的mirikizumab在治疗克罗恩病的2期临床试验中也获得了积极结果。
公司:葛兰素史克(GSK)(GSK.US)
研发投入:51亿美元
研发投入占销售额比重:12.6%

截至2019年第一季度末,GSK药物研发管线中有45款在研疗法和13款在研疫苗。该公司于去年年底收购了TESARO,并且在今年年初与德国默克达成合作协议,共同开发双特异性免疫疗法M7824。这两项举措显示出GSK公司对肿瘤学领域药物研发的重视。
在肿瘤学方面,该公司将进行多项临床试验,扩展从TESARO获得的PARP抑制剂Zejula的适用范围。该公司自主研发的靶向BCMA抗原的抗体偶联药物belantamab mafodotin(GSK2857916)在治疗复发/难治性MM患者的临床试验中获得积极结果,达到60%的ORR,其中完全缓解的患者比例达到15%。GSK预计今年将开展4项关键性临床试验,检测这一疗法治疗不同类型MM患者的疗效。
(编辑:孔文婕)



 扫码下载智通APP
扫码下载智通APP