“捡便宜”失败!这家明星机构扎堆的创新药企Menlo Therapeutics(MNLO.US),股价两年内从35美元跌至1.4美元
本文源自微信公众号“医药魔方Info”。
4月6日,专注开发皮肤科药物的Menlo Therapeutics公司(MNLO.US)宣布其NK1受体拮抗剂serlopitant治疗结节性痒疹(PN)相关瘙痒的两项III期研究(MTI-105和MTI-106)均错失了主要终点,相比安慰剂未能改善瘙痒评分。受此消息拖累,Menlo Therapeutics公司的股价大跌46%,只剩下1.4美元。两年前的4月6日,Menlo Therapeutics的股价还高达35美元。
更为糟糕的是,Menlo Therapeutics今年3月9日完成了对FoamixPharmaceuticals公司的收购。按照双方的收购协议,原Foamix股东可以每股获得0.5924股的Menlo Therapeutics公司股票,同时手握着基于serlopitant上述两项III期研究结果的对赌性股票期权(CSR)。
如果两项研究均成功,该CSR将自动作废。如果只有一项成功,原Foamix股东可以每股额外获得0.6815股的Menlo Therapeutics公司股票,届时原Foamix股东将持有Menlo Therapeutics公司全部公开发行股票的76%。如果两项研究均失败,原Foamix股东可以每股额外获得1.2082股的Menlo Therapeutics公司股票,届时将持有MenloTherapeutics公司全部公开发行股票的82%。
遗憾的是,此番大跌之后,整个Menlo
Therapeutics公司的市值也只有3400万美元了。
Menlo Therapeutics公司的前身是Tigercat Pharma,成立于2011年。这家公司自身并没有什么产品,2012年以100万美元的价格从默沙东(MRK.US)获得了MK0594的开发权益,也就是上面提到的NK-1受体拮抗剂serlopitant。默沙东当时是将MK0594作为治疗尿失禁和膀胱过度活动症的药物开发,但是因为疗效相比安慰剂并不显著,默沙东最终放弃了这款药物的开发。而Menlo Therapeutics认为MK0594应该重新拟定开发策略,选择开发用于治疗皮肤疾病相关的瘙痒,比如特应性皮炎、银屑病、结节性痒疹等。引进MK0594之后,Menlo Therapeutics公司的管线中便一直只有这一款产品,并全力推进将其开发用于治疗瘙痒和慢性咳嗽。
慢性瘙痒和慢性咳嗽影响全球数千万人,是非常有前景的适应症。Menlo Therapeutics公司在获得这款产品之后也得到了诸多投资机构的青睐,在2015-2017年间先后完成了三轮融资,之后便于2018年1月25日成功登陆纳斯达克,IPO募资1.09亿美元。在此期间,MenloTherapeutics的投资股东中大牌机构云集,包括F-Prime Capital、Novo Holdings A/S、Rock Springs Capital、Aisling Capital、Bay City Capital、venBio等,Vivo Capital在Menlo Therapeutics上市之前更是以17.3%的持股成为其最大股东。
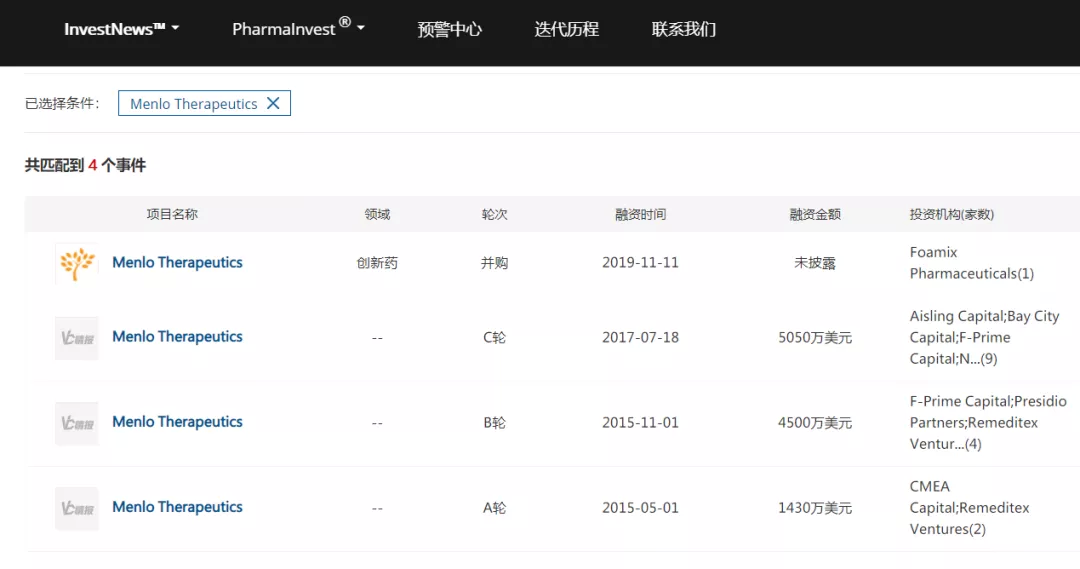
但是上市仅2个多月,MenloTherapeutics便遭遇了意外,一项涉及484例特应性皮炎相关瘙痒的II期研究失败。相比安慰剂,serlopitant在第2,4,6周三个时点均没有显著改善瘙痒评分。Menlo Therapeutics公司对此结果失望,但是仍执意要在2018年秋季在PN患者中启动III期研究,但是投资机构纷纷夺路而出,Menlo Therapeutics的股价从近40美元高点直接跌到了8美元。 此后随着2018年10月令人失望的慢性咳嗽II期临床结果公布,Menlo Therapeutics的股价再度波动下跌至不足4美元。2019年11月,Menlo Therapeutics宣布收购专注于皮肤疾病药物开发的以色列制药公司Foamix,其贫乏的产品线终于有了新成员。
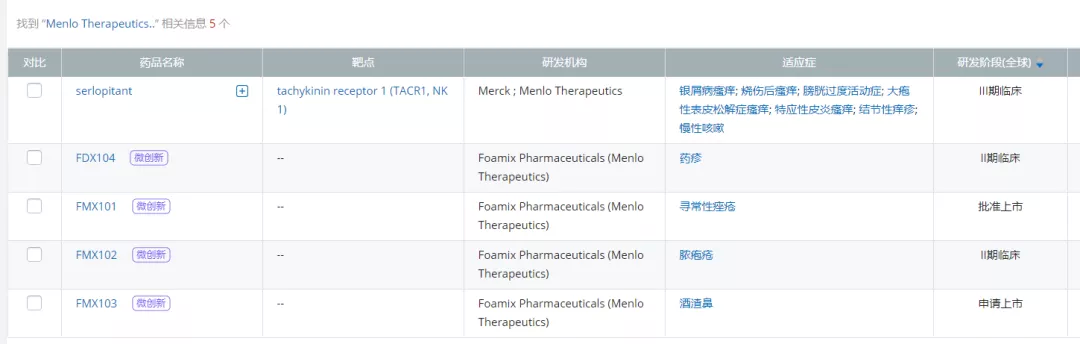
来源:NextPharma
此次遭遇失败的III期MTI-105和 MTI-106研究采用相同的试验设计,分别入组了285例和295例经历结节性痒疹(PN)直接导致的瘙痒6个月以上的患者,评估serlopitant每日1次5mg相比安慰剂的疗效和安全性差异,药物治疗时间持续10周,另设一定时间的治疗后安全性评估周期。
结果显示,MTI-105研究中serlopitant治疗组患者第10周的WI-NRS评分较基线下降4分以上的患者比例为26.45%,安慰剂组为20.31%(P=0.229)。MTI-106研究中serlopitant治疗组患者第10周的WI-NRS评分较基线下降4分以上的患者比例为25.90%,安慰剂组为18.95%(P=0.158)。针对两项研究主要终点指标的所有支持性灵敏度分析结果一致。
Menlo Therapeutics公司首席执行官 David Domzalski表示:我们为serlopitant制定了周密的III期研究计划,以评估其作为PN相关瘙痒新疗法的潜力。尽管serlopitant在数字上较安慰剂显示出了改善瘙痒的优势,但未能达到统计学意义上的显著性。我们会细致分析这些数据,希望能够对结果有进一步的理解。眼下我们会暂停推进serlopitant的临床研究,非常感谢此前参与到临床研究中的患者及其家庭,以及临床医生和医护人员。”
“尽管研究结果不利,但我们仍然致力于打造一个成功的皮肤科疾病业务,进一步扩大我们的产品管线。我们在今年初上市了治疗中重度痤疮的Amzeeq(4%米诺环素泡沫疗法),目前医生和患者的反馈和临床处方情况都很良好。FMX103(1.5%米诺环素泡沫疗法)治疗酒渣鼻的上市申请目前也正处于FDA审评之中,6月2日就将迎来结果。如果获批,这将是我们在2020年商业上市的第2款产品。此外,FCD105(米诺环素阿达帕林复方)的II期研究预计在第2季度末公布结果”,Domzalski说。
(编辑:宇硕)



 扫码下载智通APP
扫码下载智通APP